alleen voor onderzoeksdoeleinden
Cabozantinib malate VEGFR remmer
Cat.nr.S4001
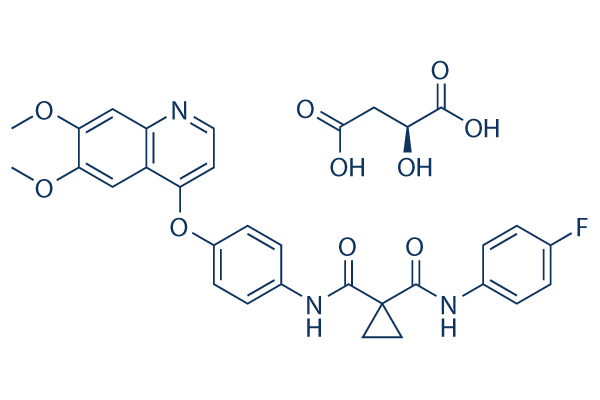
Chemische structuur
Molecuulgewicht: 635.59
Kwaliteitscontrole
| Gerelateerde doelwitten | EGFR PDGFR FGFR c-Met Src MEK CSF-1R FLT3 HER2 c-Kit |
|---|---|
| Overig VEGFR Inhibitoren | SAR131675 SU 5402 Cediranib (AZD2171) Vatalanib (PTK787) 2HCl Anlotinib (AL3818) Dihydrochloride Linifanib (ABT-869) Apatinib (YN968D1) Apatinib (YN968D1) mesylate Ki8751 ZM 323881 HCl |
Chemische informatie, opslag en stabiliteit
| Molecuulgewicht | 635.59 | Formule | C28H24FN3O5.C4H6O5 |
Opslag (vanaf de datum van ontvangst) | |
|---|---|---|---|---|---|
| CAS-nr. | 1140909-48-3 | SDF downloaden | Opslag van stamoplossingen |
|
|
| Synoniemen | XL184 | Smiles | COC1=CC2=C(C=CN=C2C=C1OC)OC3=CC=C(C=C3)NC(=O)C4(CC4)C(=O)NC5=CC=C(C=C5)F.C(C(C(=O)O)O)C(=O)O | ||
Oplosbaarheid
|
In vitro |
DMSO
: 100 mg/mL
(157.33 mM)
Water : Insoluble Ethanol : Insoluble |
Molariteitscalculator
|
In vivo |
|||||
In vivo formulatiecalculator (heldere oplossing)
Stap 1: Voer onderstaande informatie in (Aanbevolen: een extra dier om rekening te houden met verlies tijdens het experiment)
Stap 2: Voer de in vivo formulering in (Dit is alleen de calculator, geen formulering. Neem eerst contact met ons op als er geen in vivo formulering is in de sectie oplosbaarheid.)
Berekeningsresultaten:
Werkconcentratie: mg/ml;
Methode voor het bereiden van DMSO-moedervloeistof: mg geneesmiddel vooropgelost in μL DMSO ( Concentratie moedervloeistof mg/mL, Neem eerst contact met ons op als de concentratie de DMSO-oplosbaarheid van de batch van het geneesmiddel overschrijdt. )
Methode voor het bereiden van in vivo formulering: Neem μL DMSO moedervloeistof, voeg daarna toeμL PEG300, mengen en verhelderen, daarna toevoegenμL Tween 80, mengen en verhelderen, daarna toevoegen μL ddH2O, mengen en verhelderen.
Methode voor het bereiden van in vivo formulering: Neem μL DMSO moedervloeistof, voeg daarna toe μL Maïsolie, mengen en verhelderen.
Opmerking: 1. Zorg ervoor dat de vloeistof helder is voordat u het volgende oplosmiddel toevoegt.
2. Zorg ervoor dat u het/de oplosmiddel(en) in de juiste volgorde toevoegt. U moet ervoor zorgen dat de verkregen oplossing, bij de vorige toevoeging, een heldere oplossing is voordat u verdergaat met het toevoegen van het volgende oplosmiddel. Fysieke methoden zoals vortexen, ultrasoon of een warmwaterbad kunnen worden gebruikt om het oplossen te bevorderen.
Werkingsmechanisme
| Targets/IC50/Ki |
VEGFR2/KDR
(Cell-free assay) 0.035 nM
c-Met
(Cell-free assay) 1.3 nM
RET
(Cell-free assay) 4 nM
Kit
(Cell-free assay) 4.6 nM
Flt-4
(Cell-free assay) 6 nM
Axl
(Cell-free assay) 7 nM
Flt-3
(Cell-free assay) 11.3 nM
Flt-1
(Cell-free assay) 12 nM
Tie2
(Cell-free assay) 14.3 nM
|
|---|---|
| In vitro |
Cabozantinib malate heeft een zwakke remmende activiteit tegen RON en PDGFRβ met IC50's van respectievelijk 124 nM en 234 nM, en heeft een lage activiteit tegen FGFR1 met een IC50 van 5,294 μM. Dit middel in lage concentratie (0,1-0,5 μM) is voldoende om een duidelijke remming te induceren van constitutieve en induceerbare Met-fosforylering en de daaruit voortvloeiende downstream signalering in MPNST-cellen, en om HGF-geïnduceerde MPNST-celmigratie en -invasie te remmen. Het induceert ook een duidelijke remming van Met- en VEGFR2-fosforylering in cytokine-gestimuleerde menselijke navelstrengendotheelcellen (HUVEC's). Hoewel deze chemische stof geen significant effect heeft op de MPNST-celgroei bij 0,1 μM, remt het bij 5-10 μM de MPNST-celgroei significant.
|
| In vivo |
Cabozantinib malate-behandeling met 30 mg/kg bij RIP-Tag2-muizen met spontane pancreas-eilandjestumoren verstoort 83% van de tumorvascularisatie, vermindert pericyten en lege basaalmembraanhoezen, veroorzaakt wijdverspreide intratumorale hypoxie en uitgebreide tumorcelapoptose, en vertraagt de hergroei van de tumorvascularisatie na medicatie-onthouding, significant meer vergeleken met XL999 dat VEGFR blokkeert maar geen c-Met, wat leidt tot slechts 43% reductie in vascularisatie, wat suggereert dat gelijktijdige remming van VEGFR en andere functioneel relevante receptor-tyrosinekinasen (RTK) angiogeneseremming versterkt. Dit middel vermindert ook de invasiviteit van primaire tumoren en vermindert metastase. Deze chemische stof bij 30 mg/kg/dag onderdrukt significant de groei en metastase van menselijke MPNST-xenografts in SCID-muizen. Toediening van dit middel induceert dosisafhankelijke remming van tumorgroei in borst-, long- en glioomtumormodellen, in samenhang met verminderde tumor- en endotheelcelproliferatie en verhoogde apoptose. Een enkele orale dosis van deze chemische stof is voldoende om aanhoudende tumorgroeiremming te induceren bij MDA-MB-231-tumordragende muizen en C6-tumordragende ratten bij respectievelijk 100 mg/kg en 10 mg/kg.
|
Referenties |
|
Toepassingen
| Methoden | Biomarkers | Afbeeldingen | PMID |
|---|---|---|---|
| Western blot | pROS1 / pERK / pSHP2 / p-STAT3 / p-AKT p-MET / MET / p-ERK5 / ERK5 / DCLK1 |
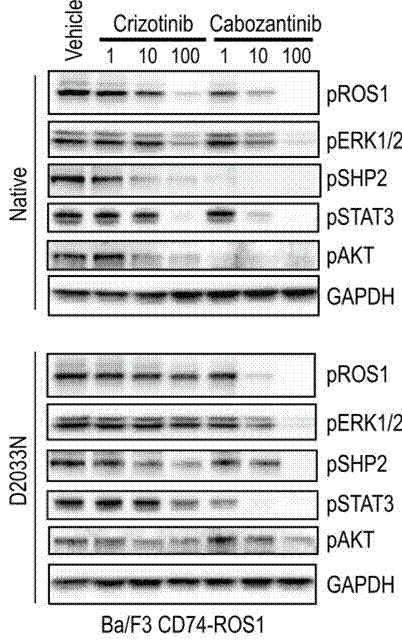
|
26673800 |
| Growth inhibition assay | Cell viability |
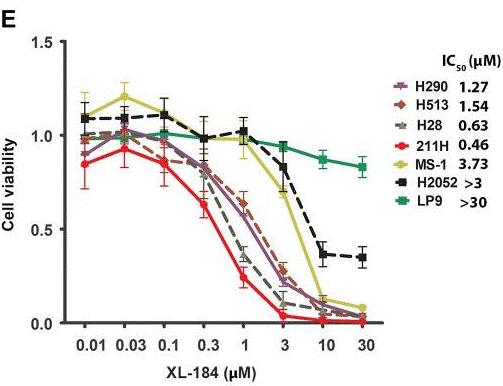
|
28560410 |
Informatie over klinische proeven
(gegevens van https://clinicaltrials.gov, bijgewerkt op 2024-05-22)
| NCT-nummer | Werving | Aandoeningen | Sponsor/medewerkers | Startdatum | Fasen |
|---|---|---|---|---|---|
| NCT06156410 | Recruiting | Ewing Sarcoma|Osteosarcoma |
Children''s Hospital of Philadelphia|Children''s Hospital Colorado|Exelixis|Alex''s Lemonade Stand Foundation |
October 24 2023 | Phase 1 |
| NCT05249114 | Active not recruiting | Neuroendocrine Tumors |
Providence Health & Services|Exelixis|Advanced Accelerator Applications SA |
December 28 2022 | Phase 1 |
| NCT05444933 | Completed | Advanced Renal Cell Carcinoma |
Ipsen |
September 16 2022 | -- |
Technische ondersteuning
Tel: +1-832-582-8158 Ext:3
Als u nog andere vragen heeft, laat dan een bericht achter.
