alleen voor onderzoeksdoeleinden
LY2109761 TGF-beta/Smad remmer
Cat.nr.S2704
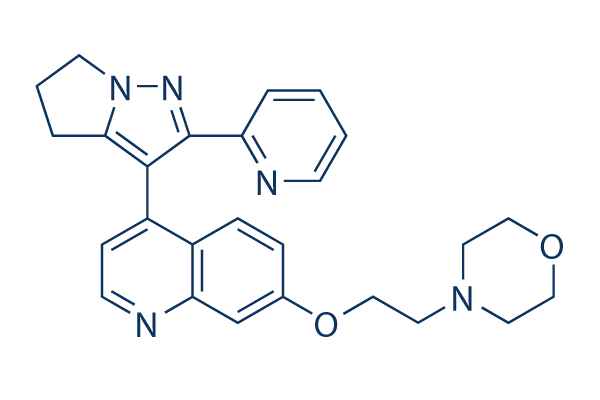
Chemische structuur
Molecuulgewicht: 441.52
Kwaliteitscontrole
Producten die vaak samen worden gebruikt met LY2109761
| Gerelateerde doelwitten | PKC ROCK Bcr-Abl |
|---|---|
| Overig TGF-beta/Smad Inhibitoren | SB431542 RepSox (E-616452) Vactosertib (TEW-7197) LDN-193189 A-83-01 LDN-193189 Dihydrochloride SRI-011381 (C381) SIS3 Hydrochloride SB-525334 DMH1 |
Celkweek, behandeling & werkzame concentratie
| Cellijnen | Assaytype | Concentratie | Incubatietijd | Formulering | Activiteitsbeschrijving | PMID |
|---|---|---|---|---|---|---|
| HepG2 | Function Assay | 10 μM | 2 h | inhibits autophagy induction by galangin | 25268046 | |
| PC-3 | Function Assay | 0.2/2/4 μM | 24 h | DMSO | inhibits TGF-β1–induced Smad2 activation | 22173053 |
| PMOs | Function Assay | 0.2/2/4 μM | 24 h | DMSO | inhibits TGF-β1–induced Smad2 activation | 22173053 |
| PC-3 | Growth Inhibition Assay | 0.2/2 μM | 24 h | DMSO | blocks the inhibition of cell proliferation produced by TGF-β1 | 22173053 |
| PMOs | Growth Inhibition Assay | 0.2/2 μM | 24 h | DMSO | blocks the inhibition of cell proliferation produced by TGF-β1 | 22173053 |
| U87MG | Growth Inhibition Assay | 5/10 μM | 2 h | enhances radiosensitivity | 22006998 | |
| T98 | Growth Inhibition Assay | 5/10 μM | 2 h | enhances radiosensitivity | 22006998 | |
| U87MG | Apoptosis Assay | 10 μM | 2 h | enhances radiation-induced DNA damage and apoptosis rates | 22006998 | |
| NMA-23 | Apoptosis Assay | 10 μM | 2 h | enhances radiation-induced DNA damage and apoptosis rates | 22006998 | |
| HLE | Function Assay | 0.01-100 nM | 48 h | inhibits the migration in a dose-dependent manner | 20844878 | |
| HLF | Function Assay | 0.01-100 nM | 48 h | inhibits the migration in a dose-dependent manner | 20844878 | |
| 10A/HER2YVMA | Growth Inhibition Assay | 0.1-0.5 μM | 9 d | reduces the size, invasiveness and cell number of colonies | 20383197 | |
| MC38 | Growth Inhibition Assay | 5 μM | 5 d | inhibits cell growth in a time-dependent manner | 19909744 | |
| U937 | Growth Inhibition Assay | 5-20 μM | 24-72 h | inhibits cell growth slightly | 18492113 | |
| HLE | Cytotoxity Assay | 0.001-20 μM | 48 h | induces cell cytotoxity in a dose-dependent manner | 18318443 | |
| HLF | Cytotoxity Assay | 0.001-20 μM | 48 h | induces cell cytotoxity in a dose-dependent manner | 18318443 | |
| Sf9 | Function assay | 1 hr | Inhibition of human His-tagged TGFbetaR1 T204D mutant expressed in Sf9 insect cells after 1 hr by HTRF assay, IC50 = 0.0037 μM. | 29422332 | ||
| Sf9 | Function assay | Inhibition of TGFbeta type receptor 1 ALK5 (T204D) expressed in Sf9 cells, IC50 = 0.069 μM. | 18314943 | |||
| Mv1Lu-p3TP-Lux | Antiproliferative assay | Antiproliferative activity against mink Mv1Lu-p3TP-Lux cells by luciferase reporter assay, IC50 = 0.18 μM. | 18314943 | |||
| NIH3T3 | Antiproliferative assay | Antiproliferative activity against mouse NIH3T3 cells by [3H]thymidine assay, IC50 = 0.21 μM. | 18314943 | |||
| Calu6 | Function assay | Inhibition of TGFbeta type receptor 1 in orally dosed human Calu6 cells xenografted mouse by IVTI pharmacokinetic assay, EC50 = 0.236 μM. | 18314943 | |||
| T-cells | Function assay | 1 hr | Inhibition of TGFbetaR1 in human primary T-cells assessed as TGFbeta-stimulated PSMAD phosphorylation preincubated for 1 hr followed by TGFbeta addition measured after 90 mins by Alpha screen assay, IC50 = 0.37 μM. | 29422332 | ||
| Mv1Lu | Function assay | 1 hr | Inhibition of TGFbetaR1 in mink Mv1Lu cells assessed as TGFbeta-stimulated PSMAD2 phosphorylation preincubated for 1 hr followed by TGFbeta addition measured after 15 mins, IC50 = 0.75 μM. | 29422332 | ||
| Klik om meer experimentele gegevens over cellijnen te bekijken | ||||||
Chemische informatie, opslag en stabiliteit
| Molecuulgewicht | 441.52 | Formule | C26H27N5O2 |
Opslag (vanaf de datum van ontvangst) | |
|---|---|---|---|---|---|
| CAS-nr. | 700874-71-1 | SDF downloaden | Opslag van stamoplossingen |
|
|
| Synoniemen | N/A | Smiles | C1CC2=C(C(=NN2C1)C3=CC=CC=N3)C4=C5C=CC(=CC5=NC=C4)OCCN6CCOCC6 | ||
Oplosbaarheid
|
In vitro |
DMSO
: 9 mg/mL
(20.38 mM)
Water : Insoluble Ethanol : Insoluble |
Molariteitscalculator
|
In vivo |
|||||
In vivo formulatiecalculator (heldere oplossing)
Stap 1: Voer onderstaande informatie in (Aanbevolen: een extra dier om rekening te houden met verlies tijdens het experiment)
Stap 2: Voer de in vivo formulering in (Dit is alleen de calculator, geen formulering. Neem eerst contact met ons op als er geen in vivo formulering is in de sectie oplosbaarheid.)
Berekeningsresultaten:
Werkconcentratie: mg/ml;
Methode voor het bereiden van DMSO-moedervloeistof: mg geneesmiddel vooropgelost in μL DMSO ( Concentratie moedervloeistof mg/mL, Neem eerst contact met ons op als de concentratie de DMSO-oplosbaarheid van de batch van het geneesmiddel overschrijdt. )
Methode voor het bereiden van in vivo formulering: Neem μL DMSO moedervloeistof, voeg daarna toeμL PEG300, mengen en verhelderen, daarna toevoegenμL Tween 80, mengen en verhelderen, daarna toevoegen μL ddH2O, mengen en verhelderen.
Methode voor het bereiden van in vivo formulering: Neem μL DMSO moedervloeistof, voeg daarna toe μL Maïsolie, mengen en verhelderen.
Opmerking: 1. Zorg ervoor dat de vloeistof helder is voordat u het volgende oplosmiddel toevoegt.
2. Zorg ervoor dat u het/de oplosmiddel(en) in de juiste volgorde toevoegt. U moet ervoor zorgen dat de verkregen oplossing, bij de vorige toevoeging, een heldere oplossing is voordat u verdergaat met het toevoegen van het volgende oplosmiddel. Fysieke methoden zoals vortexen, ultrasoon of een warmwaterbad kunnen worden gebruikt om het oplossen te bevorderen.
Werkingsmechanisme
| Targets/IC50/Ki |
TβRI
(Cell-free assay) 38 nM(Ki)
TβRII
(Cell-free assay) 300 nM(Ki)
|
|---|---|
| In vitro |
LY2109761-behandeling induceert een dosisafhankelijke groeiremming van L3.6pl/GLT-cellen met lage hechting, wat leidt tot ~33% of 73% remming bij respectievelijk 2 μM en 20 μM, wat sterk kan worden versterkt bij een combinatië-indexwaarde van 0,36581. Het blokkeren van TβRI/II-kinaseactiviteit met deze verbinding onderdrukt volledig zowel de basale als de TGF-β1-gestimuleerde migratie en invasie van L3.6pl/GLT-cellen, verhoogt de door loslating geïnduceerde apoptosis significant met 26% na 8 uur behandeling, en onderdrukt volledig de door TGF-β geïnduceerde Smad2-fosforylering. Deze chemische behandeling bij 1 nM is voldoende om de migratie en invasie, maar niet de adhesie van hepatocellulaire carcinoomcellen significant te blokkeren door de E-cadherine-expressie te verhogen. De voorbehandeling verbetert de radio gevoeligheid van glioblastoomcellen via blokkade van de TGF-β-signalering. Deze verbinding vermindert de zelfvernieuwing en proliferatie van GBM-afgeleide kankerstamcelachtige cellen (CSLC), wat significant kan worden versterkt bij combinatie met bestraling. |
| In vivo |
Toediening van LY2109761 (50 mg/kg) alleen of in combinatie vermindert het tumorvolume significant met respectievelijk ~70% en ~90%, verlengt de overleving met een mediane overlevingsduur van respectievelijk 45,0 dagen en 77,5 dagen, en vermindert spontane abdominale metastasen in het L3.6pl/GLT-xenograft-muismodel. In overeenstemming met het in vitro-effect, remt de toediening van deze verbinding alleen of in combinatie met bestraling de tumorgroei in het orthotopische CSLC-glioblastoommodel significant met respectievelijk 43,4% en 76,3%, vermindert de tumorinvasie en de dichtheid van de tumor microvaten, en verbetert de door bestraling geïnduceerde tumorgroeiachterstand significant in het U87MG-xenograft-muismodel. |
Referenties |
|
Toepassingen
| Methoden | Biomarkers | Afbeeldingen | PMID |
|---|---|---|---|
| Western blot | CDK2 / CDK4 / Cyclin D1 / p-Rb β-catenin / MMP-9 / MMP-2 / nm23 / uPA / COX-2 E-cadherin p-Smad2 / Smad |
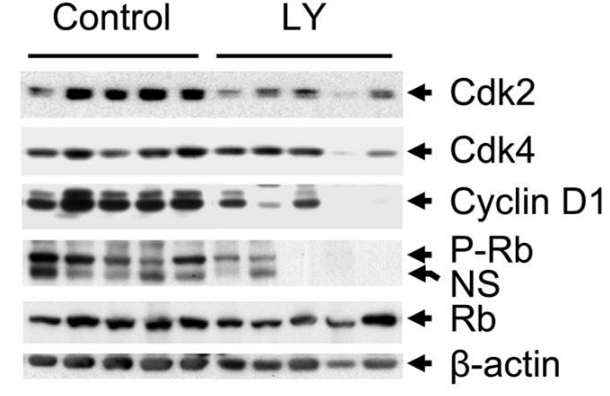
|
19909744 |
Technische ondersteuning
Tel: +1-832-582-8158 Ext:3
Als u nog andere vragen heeft, laat dan een bericht achter.
