alleen voor onderzoeksdoeleinden
b-AP15 DUB remmer
Cat.nr.S4920
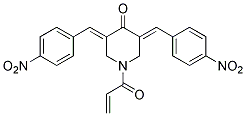
Chemische structuur
Molecuulgewicht: 419.39
Kwaliteitscontrole
| Gerelateerde doelwitten | Proteasome E1 Activating E3 Ligase p97 SUMO E2 conjugating |
|---|---|
| Overig DUB Inhibitoren | PR-619 P5091 IU1 P22077 ML323 LDN-57444 VLX1570 TCID EOAI3402143 ML364 |
Celkweek, behandeling & werkzame concentratie
| Cellijnen | Assaytype | Concentratie | Incubatietijd | Formulering | Activiteitsbeschrijving | PMID |
|---|---|---|---|---|---|---|
| P388 cells | Cytotoxicity assay | Cytotoxicity against murine P388 cells, IC50=0.05 μM | ||||
| human HSC2 | Cytotoxicity assay | Cytotoxicity against human HSC2 by MTT method, CC50=0.094 μM | ||||
| HL60 cells | Cytotoxicity assay | Cytotoxicity against human HL60 cells in presence of RPMI1640 containing 10% fetal bovine serum by trypan blue exclusion test, CC50=0.13 μM | ||||
| Molt 4/C8 cells | Cytotoxicity assay | Cytotoxicity against human Molt 4/C8 cells, IC50=0.15 μM | ||||
| CEM cells | Cytotoxicity assay | Cytotoxicity against human CEM cells, IC50=0.26 μM | ||||
| L1210 cells | Cytotoxicity assay | Cytotoxicity against murine L1210 cells, IC50=0.42 μM | ||||
| HSC4 cells | Cytotoxicity assay | Cytotoxicity against human HSC4 cells by MTT method, CC50=0.56 μM | ||||
| Klik om meer experimentele gegevens over cellijnen te bekijken | ||||||
Chemische informatie, opslag en stabiliteit
| Molecuulgewicht | 419.39 | Formule | C22H17N3O6 |
Opslag (vanaf de datum van ontvangst) | |
|---|---|---|---|---|---|
| CAS-nr. | 1009817-63-3 | SDF downloaden | Opslag van stamoplossingen |
|
|
| Synoniemen | NSC687852 | Smiles | C=CC(=O)N1CC(=CC2=CC=C(C=C2)[N+](=O)[O-])C(=O)C(=CC3=CC=C(C=C3)[N+](=O)[O-])C1 | ||
Oplosbaarheid
|
In vitro |
DMSO
: 48 mg/mL
(114.45 mM)
Water : Insoluble Ethanol : Insoluble |
Molariteitscalculator
|
In vivo |
|||||
In vivo formulatiecalculator (heldere oplossing)
Stap 1: Voer onderstaande informatie in (Aanbevolen: een extra dier om rekening te houden met verlies tijdens het experiment)
Stap 2: Voer de in vivo formulering in (Dit is alleen de calculator, geen formulering. Neem eerst contact met ons op als er geen in vivo formulering is in de sectie oplosbaarheid.)
Berekeningsresultaten:
Werkconcentratie: mg/ml;
Methode voor het bereiden van DMSO-moedervloeistof: mg geneesmiddel vooropgelost in μL DMSO ( Concentratie moedervloeistof mg/mL, Neem eerst contact met ons op als de concentratie de DMSO-oplosbaarheid van de batch van het geneesmiddel overschrijdt. )
Methode voor het bereiden van in vivo formulering: Neem μL DMSO moedervloeistof, voeg daarna toeμL PEG300, mengen en verhelderen, daarna toevoegenμL Tween 80, mengen en verhelderen, daarna toevoegen μL ddH2O, mengen en verhelderen.
Methode voor het bereiden van in vivo formulering: Neem μL DMSO moedervloeistof, voeg daarna toe μL Maïsolie, mengen en verhelderen.
Opmerking: 1. Zorg ervoor dat de vloeistof helder is voordat u het volgende oplosmiddel toevoegt.
2. Zorg ervoor dat u het/de oplosmiddel(en) in de juiste volgorde toevoegt. U moet ervoor zorgen dat de verkregen oplossing, bij de vorige toevoeging, een heldere oplossing is voordat u verdergaat met het toevoegen van het volgende oplosmiddel. Fysieke methoden zoals vortexen, ultrasoon of een warmwaterbad kunnen worden gebruikt om het oplossen te bevorderen.
Werkingsmechanisme
| Kenmerken |
Not a general deubiquitinase inhibitor. Has minimal inhibition on recombinant and cytosolic nonproteasomal cysteine deubiquitinases.
|
|---|---|
| Targets/IC50/Ki |
USP14
UCHL5
2.1 μM
|
| In vitro |
b-AP15 remt de activiteit van twee 19S-regulerende-deeltjes-geassocieerde DUBs, Ubiquitin C-terminale hydrolase 5 (UCHL5) en Ubiquitin-specific peptidase 14 (USP14), wat resulteert in accumulatie van polyubiquitine. Deze verbinding resulteert in een dosisafhankelijke accumulatie van de UbG76V-YFP-reporter met een IC50 van 0,8 μM, wat duidt op een verminderde proteasoomdegradatie. Het (1 μM) resulteert in snelle accumulatie van polyubiquitineerde eiwitten in menselijke coloncarcinoom HCT-116 cellen. Dit chemische middel (2,2 μM) verhoogt de hoeveelheden van de cycline-afhankelijke kinasen CDKN1A en CDKNIB en de tumorsuppressor TP53 op een dosisafhankelijke manier zonder de hoeveelheden ornithine decarboxylase 1 (ODC1) in HCT-116 cellen te veranderen. Het (1 μM) resulteert in G2/M fase celcyclusarrest in HCT-116 cellen, consistent met de accumulatie van celcyclusremmers. Deze behandeling met de verbinding verhoogt het aantal hypodiploïde cellen en wordt geassocieerd met verhoogde hoeveelheden apoptotische markers, waaronder geactiveerd caspase-3, caspase-gesplitste poly-ADP ribose polymerase (PARP) en cytokeratine-18 (CK18). Het is toxischer voor HCT-116 cellen vergeleken met geïmmortaliseerde epitheelcellen (hTERT-RPE1) of perifere bloedmononucleaire cellen. Deze remmer remt de deubiquitinerende activiteit met behulp van een verscheidenheid aan substraten, waaronder Ub-AMC, Ub-GFP22, ubiquitineerd p53-bindend proteïnehomoloog (HDM2), en K48- en K63-gekoppelde Ubiquitin tetramere ketens. Het is een remmer van het UPS die celdood induceerde via inductie van de lysosomale apoptoseroute op een cathepsine-D afhankelijke manier. Deze verbinding veroorzaakt karakteristieke UPS-defecten, waaronder de accumulatie van Ubiquitin-conjugaten en celcyclusremmers zoals p21, p27 en de tumorsuppressor p53. Het remt de DUB-activiteit van beide cysteïne DUBs, waarbij USP14 iets gevoeliger is dan UCHL5. Dit chemische middel induceert apoptose in cellen die het anti-apoptotische Bcl-2-eiwit overexpressie vertonen en in cellen die het p53-gen missen. Het (1 μM) remt ATP-geïnduceerde IL-1β-afgifte van LPS-geprimeerde peritoneale macrofagen. Deze verbinding (1 μM) vermindert de niveaus van celdood geïnduceerd door nigericinebehandeling in THP-1 cellen. Het (1 μM) vermindert significant het aantal ASC-specks gevormd na nigericinebehandeling in LPS-geprimeerde THP-1 cellen.
|
| In vivo |
b-AP15 (5 mg/kg) vertoont significante antitumoractiviteit bij SCID-muizen met FaDu plaveiselcarcinoom xenotransplantaten. Deze verbinding vertraagt significant de tumoronset bij muizen met HCT-116 coloncarcinoom xenotransplantaten.
|
Referenties |
|
Technische ondersteuning
Tel: +1-832-582-8158 Ext:3
Als u nog andere vragen heeft, laat dan een bericht achter.
