alleen voor onderzoeksdoeleinden
TIC10 (ONC201) Akt remmer
Cat.nr.S7963
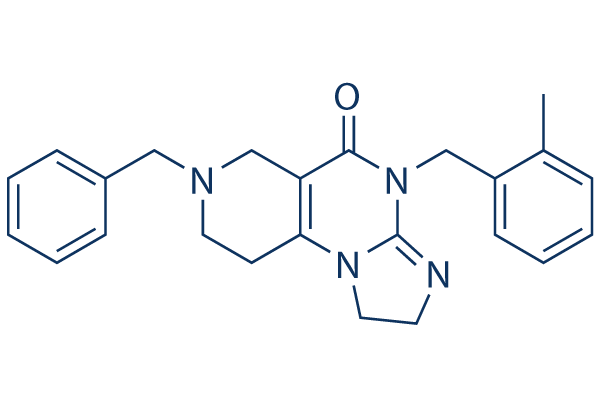
Chemische structuur
Molecuulgewicht: 386.49
Kwaliteitscontrole
| Gerelateerde doelwitten | PI3K mTOR GSK-3 ATM/ATR DNA-PK AMPK PDPK1 PTEN PP2A PDK |
|---|---|
| Overig Akt Inhibitoren | SC79 AZD5363 (Capivasertib) MK-2206 Dihydrochloride Ipatasertib (GDC-0068) Perifosine GSK690693 Triciribine (API-2) Afuresertib (GSK2110183) CCT128930 A-674563 HCl |
Chemische informatie, opslag en stabiliteit
| Molecuulgewicht | 386.49 | Formule | C24H26N4O |
Opslag (vanaf de datum van ontvangst) | |
|---|---|---|---|---|---|
| CAS-nr. | 1616632-77-9 | SDF downloaden | Opslag van stamoplossingen |
|
|
| Synoniemen | N/A | Smiles | CC1=CC=CC=C1CN2C(=O)C3=C(CCN(C3)CC4=CC=CC=C4)N5C2=NCC5 | ||
Oplosbaarheid
|
In vitro |
DMSO
: 77 mg/mL
(199.22 mM)
Ethanol : 77 mg/mL Water : Insoluble |
Molariteitscalculator
|
In vivo |
|||||
In vivo formulatiecalculator (heldere oplossing)
Stap 1: Voer onderstaande informatie in (Aanbevolen: een extra dier om rekening te houden met verlies tijdens het experiment)
Stap 2: Voer de in vivo formulering in (Dit is alleen de calculator, geen formulering. Neem eerst contact met ons op als er geen in vivo formulering is in de sectie oplosbaarheid.)
Berekeningsresultaten:
Werkconcentratie: mg/ml;
Methode voor het bereiden van DMSO-moedervloeistof: mg geneesmiddel vooropgelost in μL DMSO ( Concentratie moedervloeistof mg/mL, Neem eerst contact met ons op als de concentratie de DMSO-oplosbaarheid van de batch van het geneesmiddel overschrijdt. )
Methode voor het bereiden van in vivo formulering: Neem μL DMSO moedervloeistof, voeg daarna toeμL PEG300, mengen en verhelderen, daarna toevoegenμL Tween 80, mengen en verhelderen, daarna toevoegen μL ddH2O, mengen en verhelderen.
Methode voor het bereiden van in vivo formulering: Neem μL DMSO moedervloeistof, voeg daarna toe μL Maïsolie, mengen en verhelderen.
Opmerking: 1. Zorg ervoor dat de vloeistof helder is voordat u het volgende oplosmiddel toevoegt.
2. Zorg ervoor dat u het/de oplosmiddel(en) in de juiste volgorde toevoegt. U moet ervoor zorgen dat de verkregen oplossing, bij de vorige toevoeging, een heldere oplossing is voordat u verdergaat met het toevoegen van het volgende oplosmiddel. Fysieke methoden zoals vortexen, ultrasoon of een warmwaterbad kunnen worden gebruikt om het oplossen te bevorderen.
Werkingsmechanisme
| Targets/IC50/Ki |
Akt
ERK
|
|---|---|
| In vitro |
Op een p53-onafhankelijke manier veroorzaakt TIC10 (ONC201) een dosisafhankelijke toename van TRAIL mRNA en induceert het TRAIL-eiwitlokalisatie op het celoppervlak van verschillende kankercellijnen. Het heeft een breed spectrum activiteit tegen meerdere maligniteiten in vitro en induceert een toename van sub-G1 DNA-gehalte, wat wijst op celdood in TRAIL-gevoelige HCT116 p53−/− cellen, maar verandert de celcyclusprofielen van normale fibroblasten niet bij equivalente doses. Deze verbinding vermindert de clonogene overleving van kankercellijnen en spaart normale fibroblasten. Het verhoogt het percentage sub-G1 DNA in kankercellen op een p53-onafhankelijke en Bax-afhankelijke manier, zoals eerder gemeld voor TRAIL-gemedieerde Apoptosis. TIC10-geïnduceerde TRAIL-opregulatie is Foxo3a-afhankelijk, wat ook TRAIL-doodreceptor DR5 opreguleert naast andere doelen, waardoor mogelijk enkele TRAIL-resistente tumorcellen gesensibiliseerd kunnen worden. Het middel inactiveert kinasen Akt en extracellulaire signaal–gereguleerde kinase (ERK), wat leidt tot de translocatie van Foxo3a naar de kern, waar het bindt aan de TRAIL-promotor om de gen transcriptie op te reguleren. Het is een doeltreffend antitumor therapeutisch middel dat inwerkt op tumorcellen en hun micro-omgeving om de concentraties van de endogene tumorsuppressor TRAIL te verhogen. |
| In vivo |
In het HCT116 p53−/− xenograft veroorzaakt behandeling met TIC10 (ONC201) en TRAIL tumorregressie in een vergelijkbare mate wanneer beide als meerdere doses worden toegediend. Het induceert ook regressie van MDA-MB-231 humane triple-negatieve borstkanker xenografts, terwijl TRAIL-behandelde tumoren progresseerden. In DLD-1 darmkanker xenografts induceert dit compound tumorstase 1 week na behandeling, terwijl TRAIL-behandelde tumoren progressie vertonen na een enkele dosis. Een enkele dosis ervan induceert ook een aanhoudende regressie van het SW480 xenograft en is even effectief wanneer toegediend via intraperitoneale of orale route, wat een gunstige orale biologische beschikbaarheid suggereert. Het veroorzaakt tumorspecifieke celdood door TRAIL-gemedieerde directe en omstandereffecten en is een effectief antitumor middel tegen orthotope humane glioblastoma multiforme tumoren. |
Referenties |
|
Toepassingen
| Methoden | Biomarkers | Afbeeldingen | PMID |
|---|---|---|---|
| Western blot | Cleaved PARP / CC3 ATF4 / ATF3 p-GCN2 / GCN2 / p-eIF2a / eIF2a p-p70S6K / p-S6 / p-4EBP1 / 4EBP1 / p-HSF1 / HSF1 |
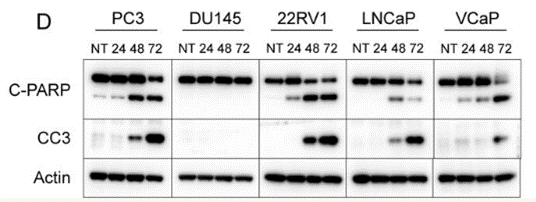
|
29588331 |
| Growth inhibition assay | Cell viability |
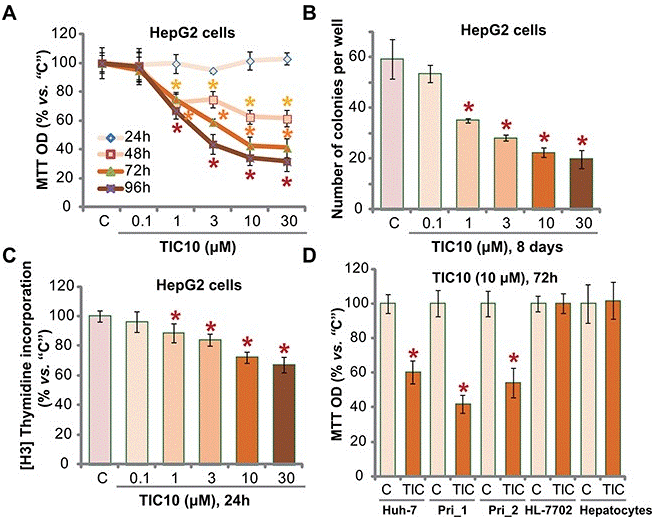
|
29588330 |
Informatie over klinische proeven
(gegevens van https://clinicaltrials.gov, bijgewerkt op 2024-05-22)
| NCT-nummer | Werving | Aandoeningen | Sponsor/medewerkers | Startdatum | Fasen |
|---|---|---|---|---|---|
| NCT04629209 | Withdrawn | Glioblastoma |
Masonic Cancer Center University of Minnesota|University of Minnesota |
June 28 2024 | Phase 2 |
| NCT06012929 | Not yet recruiting | Meningioma|Refractory Meningioma|Relapsed Meningioma |
University of Nebraska|Chimerix |
April 2024 | Phase 1 |
| NCT05476939 | Recruiting | Diffuse Intrinsic Pontine Glioma|Diffuse Midline Glioma H3 K27M-Mutant |
Gustave Roussy Cancer Campus Grand Paris|Chimerix|Innovative Therapies For Children with Cancer Consortium |
September 29 2022 | Phase 3 |
Technische ondersteuning
Tel: +1-832-582-8158 Ext:3
Als u nog andere vragen heeft, laat dan een bericht achter.
