alleen voor onderzoeksdoeleinden
Deguelin Akt remmer
Cat.nr.S8132
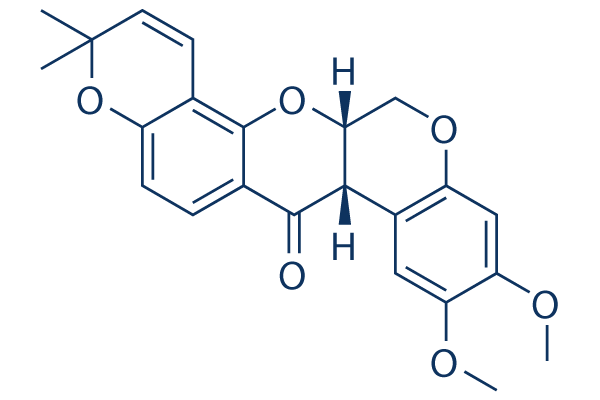
Chemische structuur
Molecuulgewicht: 394.42
Kwaliteitscontrole
| Gerelateerde doelwitten | PI3K mTOR GSK-3 ATM/ATR DNA-PK AMPK PDPK1 PTEN PP2A PDK |
|---|---|
| Overig Akt Inhibitoren | SC79 AZD5363 (Capivasertib) MK-2206 Dihydrochloride Ipatasertib (GDC-0068) Perifosine GSK690693 Triciribine (API-2) Afuresertib (GSK2110183) CCT128930 A-674563 HCl |
Chemische informatie, opslag en stabiliteit
| Molecuulgewicht | 394.42 | Formule | C23H22O6 |
Opslag (vanaf de datum van ontvangst) | |
|---|---|---|---|---|---|
| CAS-nr. | 522-17-8 | SDF downloaden | Opslag van stamoplossingen |
|
|
| Synoniemen | (-)-Deguelin, (-)-cis-Deguelin | Smiles | CC1(C=CC2=C(O1)C=CC3=C2OC4COC5=CC(=C(C=C5C4C3=O)OC)OC)C | ||
Oplosbaarheid
|
In vitro |
DMSO
: 78 mg/mL
(197.75 mM)
Ethanol : 78 mg/mL Water : Insoluble |
Molariteitscalculator
|
In vivo |
|||||
In vivo formulatiecalculator (heldere oplossing)
Stap 1: Voer onderstaande informatie in (Aanbevolen: een extra dier om rekening te houden met verlies tijdens het experiment)
Stap 2: Voer de in vivo formulering in (Dit is alleen de calculator, geen formulering. Neem eerst contact met ons op als er geen in vivo formulering is in de sectie oplosbaarheid.)
Berekeningsresultaten:
Werkconcentratie: mg/ml;
Methode voor het bereiden van DMSO-moedervloeistof: mg geneesmiddel vooropgelost in μL DMSO ( Concentratie moedervloeistof mg/mL, Neem eerst contact met ons op als de concentratie de DMSO-oplosbaarheid van de batch van het geneesmiddel overschrijdt. )
Methode voor het bereiden van in vivo formulering: Neem μL DMSO moedervloeistof, voeg daarna toeμL PEG300, mengen en verhelderen, daarna toevoegenμL Tween 80, mengen en verhelderen, daarna toevoegen μL ddH2O, mengen en verhelderen.
Methode voor het bereiden van in vivo formulering: Neem μL DMSO moedervloeistof, voeg daarna toe μL Maïsolie, mengen en verhelderen.
Opmerking: 1. Zorg ervoor dat de vloeistof helder is voordat u het volgende oplosmiddel toevoegt.
2. Zorg ervoor dat u het/de oplosmiddel(en) in de juiste volgorde toevoegt. U moet ervoor zorgen dat de verkregen oplossing, bij de vorige toevoeging, een heldere oplossing is voordat u verdergaat met het toevoegen van het volgende oplosmiddel. Fysieke methoden zoals vortexen, ultrasoon of een warmwaterbad kunnen worden gebruikt om het oplossen te bevorderen.
Werkingsmechanisme
| Targets/IC50/Ki |
PI3K
Akt
|
|---|---|
| In vitro |
Deguelin downreguleert Akt-fosforylering in leukemiecellijnen met een actieve PI3K/Akt-as. Bij 10 of 100 nmol/l is deze verbinding effectief in het remmen van Akt-fosforylering. De totale Akt-expressie wordt er niet door veranderd. Bovendien beïnvloedt het de expressie of de fosforyleringsniveaus van p44/42 of p38 MAP-kinasen in U937-cellen niet. Het verhoogt de gevoeligheid van menselijke leukemiecellen voor chemotherapeutische middelen. Deze chemische stof defosforyleert Akt en verhoogt de cytarabine-gevoeligheid van AML-blasten, maar niet van CB CD34+. Het veroorzaakt, indien gedurende 24 uur bij 10 nmol/l gebruikt, een S-fase-arrest van U937-cellen, met interferentie van de progressie naar de G2/M-fase. Indien het alleen wordt gebruikt tot een concentratie van 10 nmol/l gedurende 24 uur, verhoogt het de apoptotische snelheid van U937-cellen niet significant.
|
| In vivo |
Deguelin remt in vivo angiogenese van het chorionallantoismembraan (CAM) van kuikens zonder cytotoxisch effect en vermindert significant laser-geïnduceerde CNV in een muismodel van AMD zonder significante retinale toxiciteit. Het vertoonde significante anti-tumorigenese en anti-proliferatieve activiteit in verschillende soorten kanker, zowel in vitro als in vivo. In preklinische proeven verminderde deze verbinding de tumorincidentie aanzienlijk. Topisch toegediende deguelin onderdrukte significant de multipliciteit van huidtumoren met UVB-inductie, wat wijst op het effect als een potentieel kankerchemopreventief middel. Bij A/J-muizen verminderde deze chemische stof duidelijk de tumormultipliciteit en het volume, evenals de algehele tumorlast bij blootstelling aan het tabaksspecifieke carcinogeen benzo(a)pyreen (Bap) en andere carcinogenen, zonder detecteerbare toxiciteit. Desalniettemin mag de toxiciteit van deze verbinding boven een bepaalde dosis niet worden verwaarloosd. Behandeling met deguelin, een potentiële mitochondriale complex I-remmer, verminderde tyrosinehydroxylase-positieve neuronen, wat leidde tot de ziekte van Parkinson. Kim et al. tonen aan dat deze chemische stof een PD-achtig syndroom bevorderde, voornamelijk via Src/STAT-signalering, aangezien α-synucleïne (een belangrijke eiwitfunctie in de pathogenese van PD) werd gefosforyleerd door deguelin-geactiveerd Src.
|
Referenties |
|
Technische ondersteuning
Tel: +1-832-582-8158 Ext:3
Als u nog andere vragen heeft, laat dan een bericht achter.
