alleen voor onderzoeksdoeleinden
Mifepristone (RU-486) Progesteronreceptorantagonist
Cat.nr.S2606
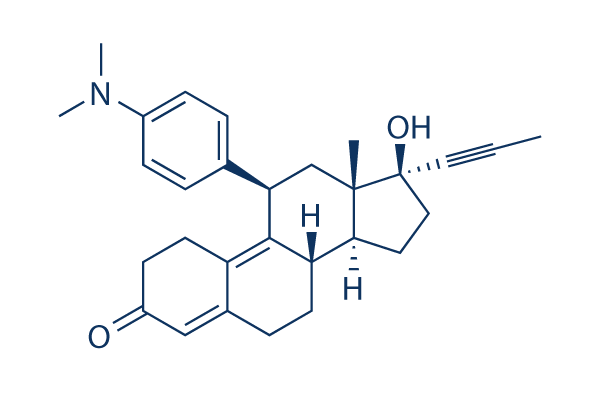
Chemische structuur
Molecuulgewicht: 429.59
Kwaliteitscontrole
| Gerelateerde doelwitten | Adrenergic Receptor GPR Androgen Receptor Glucocorticoid Receptor ACE RAAS Progesterone Receptor Opioid Receptor PGES THR |
|---|---|
| Overig Estrogen/progestogen Receptor Inhibitoren | Elacestrant (RAD1901) Dihydrochloride Vepdegestrant (ARV-471) MPP dihydrochloride Kaempferol Cholesterol G15 Endoxifen HCl Licochalcone A Chrysin Pregnenolone |
Celkweek, behandeling & werkzame concentratie
| Cellijnen | Assaytype | Concentratie | Incubatietijd | Formulering | Activiteitsbeschrijving | PMID |
|---|---|---|---|---|---|---|
| CHO-K1 cells | Function assay | Inhibition of CHO-K1 cells expressing glucocorticoid receptor, IC50=8e-06 μM | ||||
| T47D-C124 cells | Function assay | 24 h | Antagonist activity at progesterone receptor in human T47D-C124 cells transfected with luciferase gene linked to MMTV promoter assessed as inhibition of progesterone-induced luciferase transactivation activity after 24 hrs, IC50=2.1e-05 μM | |||
| neuroblastoma cells | Function assay | In vitro antagonist potency in transactivation assay in neuroblastoma cells expressing human PR-B progesterone receptor, IC50=2.5e-05 μM | ||||
| T47D cells | Function assay | 48 h | Antagonist activity at progesterone receptor in human T47D cells assessed as inhibition of progesterone-induced alkaline phosphatase activity after 48 hrs, IC50=4.5e-05 μM | |||
| CV-1 cells | Function assay | Antagonistic activity against human progesterone receptor B (hPR-B) in co-transfected CV-1 cells, IC50=0.00018 μM | ||||
| HEK293 cells | Function assay | Antagonist activity against glucocorticoid receptor (unknown origin) expressed in HEK293 cells by GRE-dependent luciferase reporter gene assay, IC50=0.000298 μM | ||||
| COS7 cells | Function assay | Antagonist activity at cloned glucocorticoid receptor-ligand binding domain expressed in african green monkey COS7 cells by GAL4 luciferase reporter assay, IC50=0.0006 μM | ||||
| SW1353 cells | Function assay | Binding affinity to glucocorticoid receptor in SW1353 cells by whole-cell binding assay, Ki=0.00082 μM | ||||
| A549 cells | Function assay | Antagonist activity at human glucocorticoid receptor assessed as inhibition of corticoid-induced transcription in human A549 cells by GRE-linked luciferase reporter gene assay, IC50=0.0016 μM | ||||
| A549 cells | Function assay | 16 h | Antagonist activity at glucocorticoid receptor in human A549 cells assessed as inhibition of corticoid-induced transcription after 16 hrs by glucocorticoid response element-driven luciferase reporter gene assay, IC50=0.0016 μM | |||
| rat H4-IIE cells | Function assay | 1 h | Antagonist activity against glucocorticoid receptor in rat H4-IIE cells assessed as inhibition of dexamethasone-induced receptor transactivation pre-incubated for 1 hr before dexamethasone addition and measured 24 hrs post dexamethasone stimulation by tyrosine aminotransferase enzyme assay, IC50=0.00194 μM | |||
| HeLa cells | Function assay | Effective concentration against inhibition of Dexamethasone induced glucocorticoid receptor transactivation of mouse mammary tumor virus luciferase gene in HeLa cells, EC50=0.002 μM | ||||
| NIH3T3 cells | Function assay | In vitro antagonist potency in transactivation assay in NIH3T3 cells expressing glucocorticoid receptor, IC50=0.0022 μM | ||||
| CHO cells | Function assay | Inhibition of Dexamethasone stimulated transcriptional activity in CHO cells expressing glucocorticoid receptor, IC50=0.005 μM | ||||
| hGRAF cells | Function assay | Inhibition of human GR expressed in hGRAF cells, Ki=0.005 μM | ||||
| COS-1 | Function assay | Binding affinity for human androgen receptor in transiently-transfected COS-1 cells, Ki=0.022 μM | ||||
| rat hepatocytes | Function assay | Inhibition of dexamethasone-induced GR-mediated tyrosine amino transferase activity in rat hepatocytes, IC50=0.27 μM | ||||
| human K562/R7 cells | Function assay | 72 h | Potentiation of doxorubicin-induced cytotoxicity against doxorubicin-resistant human K562/R7 cells assessed as doxorubicin IC50 at 1 uM after 72 hrs by MTT assay, IC50=0.9 μM | |||
| Klik om meer experimentele gegevens over cellijnen te bekijken | ||||||
Chemische informatie, opslag en stabiliteit
| Molecuulgewicht | 429.59 | Formule | C29H35NO2 |
Opslag (vanaf de datum van ontvangst) | |
|---|---|---|---|---|---|
| CAS-nr. | 84371-65-3 | SDF downloaden | Opslag van stamoplossingen |
|
|
| Synoniemen | C-1073, RU 38486 | Smiles | CC#CC1(CCC2C1(CC(C3=C4CCC(=O)C=C4CCC23)C5=CC=C(C=C5)N(C)C)C)O | ||
Oplosbaarheid
|
In vitro |
DMSO
: 85 mg/mL
(197.86 mM)
Ethanol : 85 mg/mL Water : Insoluble |
Molariteitscalculator
|
In vivo |
|||||
In vivo formulatiecalculator (heldere oplossing)
Stap 1: Voer onderstaande informatie in (Aanbevolen: een extra dier om rekening te houden met verlies tijdens het experiment)
Stap 2: Voer de in vivo formulering in (Dit is alleen de calculator, geen formulering. Neem eerst contact met ons op als er geen in vivo formulering is in de sectie oplosbaarheid.)
Berekeningsresultaten:
Werkconcentratie: mg/ml;
Methode voor het bereiden van DMSO-moedervloeistof: mg geneesmiddel vooropgelost in μL DMSO ( Concentratie moedervloeistof mg/mL, Neem eerst contact met ons op als de concentratie de DMSO-oplosbaarheid van de batch van het geneesmiddel overschrijdt. )
Methode voor het bereiden van in vivo formulering: Neem μL DMSO moedervloeistof, voeg daarna toeμL PEG300, mengen en verhelderen, daarna toevoegenμL Tween 80, mengen en verhelderen, daarna toevoegen μL ddH2O, mengen en verhelderen.
Methode voor het bereiden van in vivo formulering: Neem μL DMSO moedervloeistof, voeg daarna toe μL Maïsolie, mengen en verhelderen.
Opmerking: 1. Zorg ervoor dat de vloeistof helder is voordat u het volgende oplosmiddel toevoegt.
2. Zorg ervoor dat u het/de oplosmiddel(en) in de juiste volgorde toevoegt. U moet ervoor zorgen dat de verkregen oplossing, bij de vorige toevoeging, een heldere oplossing is voordat u verdergaat met het toevoegen van het volgende oplosmiddel. Fysieke methoden zoals vortexen, ultrasoon of een warmwaterbad kunnen worden gebruikt om het oplossen te bevorderen.
Werkingsmechanisme
| Kenmerken |
Mifepristone is the first approved medication for patients with endogenous cushing
|
|---|---|
| Targets/IC50/Ki |
Bcl-2
Progesterone receptor
(T47D cells) 0.2 nM
Glucocorticoid receptor
(A549 cells) 2.6 nM
|
| In vitro |
Mifepristone remt cortico de-ge nduceerde transcriptie van een glucocortico de respons element (GRE)-gekoppeld luciferase reportergen in de menselijke longcarcinoomcellijn A549. Bovendien blokkeert deze verbinding ook de progesteron-inductie van alkalische fosfatase-activiteit in de menselijke borstkankercellijn T47D. Het remt de groei van eierstokkankercellen van SK-OV-3 en OV2008 met IC50 van respectievelijk 6,25 M en 6,91 M. Een recente studie toont aan dat deze chemische stof caspase-1 overexpressie induceert in zowel gedifferentieerde als ongedifferentieerde caspase-1-embryonale stamcellen. |
| Kinase Assay |
Glucocortico
de receptor (GR) antagonistische activiteit, Progesteron receptor (PR) antagonistische activiteit
|
|
T47D alkalische fosfatase-test: T47D menselijke borstkankercellen worden ge
platooid in 96-wells weefselkweekplaten met 104 cellen per putje in assaymedium [RPMI-medium zonder fenolrood dat 5% (v/v) met houtskool behandeld FBS en 1% (v/v) penicilline-streptomycine bevat]. Twee dagen later wordt het medium afgegoten en wordt Mifepristone of controle toegevoegd in een eindconcentratie in vers assaymedium. Vierentwintig uur later wordt een alkalische fosfatase-test uitgevoerd met behulp van een SEAP-kit. Het medium wordt afgegoten en de cellen worden gedurende 30 minuten bij kamertemperatuur gefixeerd met 5% (v/v) formaline. De cellen worden
nmaal bij kamertemperatuur gewassen met Hanks
|
|
| In vivo |
Mifepristone kan de groei van SK-OV-3 tumoren in immunosuppressieve muizen bij 0,5 mg/dag en 1 mg/dag belemmeren. Deze verbinding remt het prostaatgewicht significant bij de hoogste doses in vivo, en remt de groei van de prostaatklier geproduceerd door dihydrotestosteron (DHT) in grotere mate dan de inductie van atrofie en celdood bij ratten. |
Referenties |
|
Toepassingen
| Methoden | Biomarkers | Afbeeldingen | PMID |
|---|---|---|---|
| Western blot | p-AKT / AKT / p-ERK / ERK MMP-2 / MMP-9 / COX-2 / VEGF |
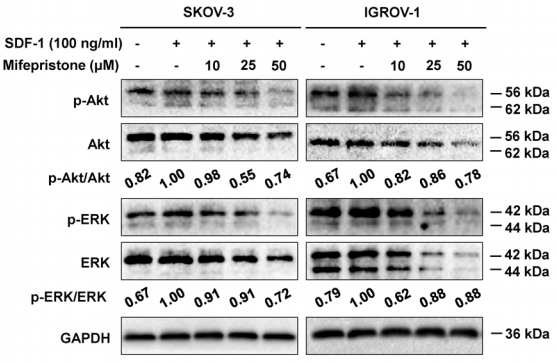
|
28938623 |
Informatie over klinische proeven
(gegevens van https://clinicaltrials.gov, bijgewerkt op 2024-05-22)
| NCT-nummer | Werving | Aandoeningen | Sponsor/medewerkers | Startdatum | Fasen |
|---|---|---|---|---|---|
| NCT06394999 | Not yet recruiting | Female Contraception |
Leiden University Medical Center|Karolinska Institutet|Women on Waves|Children''s Investment Fund Foundation |
September 2024 | Phase 3 |
| NCT05177510 | Recruiting | Labor Induced |
Chelsea and Westminster NHS Foundation Trust |
August 25 2023 | Phase 3 |
| NCT04905251 | Recruiting | Medical Abortion |
Linepharma International LTD |
February 22 2022 | -- |
| NCT05062174 | Withdrawn | BRCA1 Mutation|High-grade Serous Ovarian Cancer|TNBC - Triple-Negative Breast Cancer |
Indiana University|Breast Cancer Research Foundation |
November 1 2021 | -- |
| NCT04588688 | Terminated | Central Adrenal Insufficiency|Mifepristone |
Tobias Else|Corcept Therapeutics|University of Michigan |
May 5 2021 | Phase 2 |
| NCT03659045 | Completed | Abortion-Related Disorders |
Assistance Publique Hopitaux De Marseille |
January 15 2019 | Not Applicable |
Technische ondersteuning
Tel: +1-832-582-8158 Ext:3
Als u nog andere vragen heeft, laat dan een bericht achter.
