alleen voor onderzoeksdoeleinden
Fasiglifam(TAK-875) Hemihydrate GPR agonist
Cat.nr.S2637
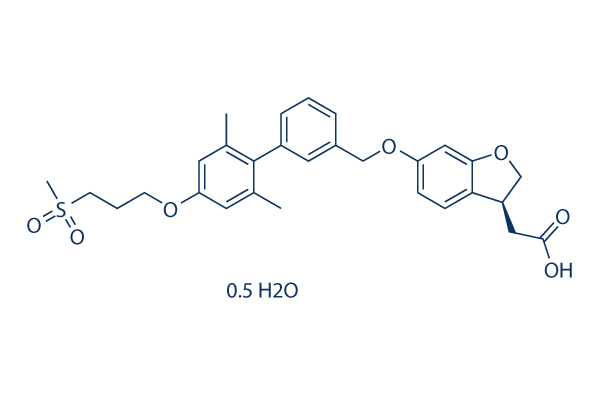
Chemische structuur
Molecuulgewicht: 533.63
Kwaliteitscontrole
| Gerelateerde doelwitten | Adrenergic Receptor Estrogen/progestogen Receptor Androgen Receptor Glucocorticoid Receptor ACE RAAS Progesterone Receptor Opioid Receptor PGES THR |
|---|---|
| Overig GPR Inhibitoren | ONC212 GW9508 AH7614 3-chloro-5-hydroxybenzoic Acid JMS-17-2 GSK1292263 AZD1981 TC-G-1008 (GPR39-C3) SNAP94847 hydrochloride 6-OAU |
Celkweek, behandeling & werkzame concentratie
| Cellijnen | Assaytype | Concentratie | Incubatietijd | Formulering | Activiteitsbeschrijving | PMID |
|---|---|---|---|---|---|---|
| human 1321N1 cells | Function assay | Agonist activity at human FFA1 receptor expressed in human 1321N1 cells assessed as calcium mobilization by fluorescence spectrophotometry, EC50=14.13 nM | ||||
| CHO cells | Function assay | Agonist activity at human GP40 receptor expressed in CHO cells assessed as increase in intracellular calcium level for 90 secs by FLIPR assay in the presence of 0.1% BSA, EC50=0.016 μM | ||||
| Klik om meer experimentele gegevens over cellijnen te bekijken | ||||||
Chemische informatie, opslag en stabiliteit
| Molecuulgewicht | 533.63 | Formule | C29H32O7S.1/2H2O |
Opslag (vanaf de datum van ontvangst) | |
|---|---|---|---|---|---|
| CAS-nr. | 1374598-80-7 | SDF downloaden | Opslag van stamoplossingen |
|
|
| Synoniemen | N/A | Smiles | CC1=CC(=CC(=C1C2=CC=CC(=C2)COC3=CC4=C(C=C3)C(CO4)CC(=O)O)C)OCCCS(=O)(=O)C.CC1=CC(=CC(=C1C2=CC=CC(=C2)COC3=CC4=C(C=C3)C(CO4)CC(=O)O)C)OCCCS(=O)(=O)C.O | ||
Oplosbaarheid
|
In vitro |
DMSO
: 100 mg/mL
(187.39 mM)
Water : Insoluble Ethanol : Insoluble |
Molariteitscalculator
|
In vivo |
|||||
In vivo formulatiecalculator (heldere oplossing)
Stap 1: Voer onderstaande informatie in (Aanbevolen: een extra dier om rekening te houden met verlies tijdens het experiment)
Stap 2: Voer de in vivo formulering in (Dit is alleen de calculator, geen formulering. Neem eerst contact met ons op als er geen in vivo formulering is in de sectie oplosbaarheid.)
Berekeningsresultaten:
Werkconcentratie: mg/ml;
Methode voor het bereiden van DMSO-moedervloeistof: mg geneesmiddel vooropgelost in μL DMSO ( Concentratie moedervloeistof mg/mL, Neem eerst contact met ons op als de concentratie de DMSO-oplosbaarheid van de batch van het geneesmiddel overschrijdt. )
Methode voor het bereiden van in vivo formulering: Neem μL DMSO moedervloeistof, voeg daarna toeμL PEG300, mengen en verhelderen, daarna toevoegenμL Tween 80, mengen en verhelderen, daarna toevoegen μL ddH2O, mengen en verhelderen.
Methode voor het bereiden van in vivo formulering: Neem μL DMSO moedervloeistof, voeg daarna toe μL Maïsolie, mengen en verhelderen.
Opmerking: 1. Zorg ervoor dat de vloeistof helder is voordat u het volgende oplosmiddel toevoegt.
2. Zorg ervoor dat u het/de oplosmiddel(en) in de juiste volgorde toevoegt. U moet ervoor zorgen dat de verkregen oplossing, bij de vorige toevoeging, een heldere oplossing is voordat u verdergaat met het toevoegen van het volgende oplosmiddel. Fysieke methoden zoals vortexen, ultrasoon of een warmwaterbad kunnen worden gebruikt om het oplossen te bevorderen.
Werkingsmechanisme
| Kenmerken |
More potent at activating hGPR40 than oleic acid.
|
|---|---|
| Targets/IC50/Ki |
GPR40
(CHO cells expressing human GPR40) 14 nM(EC50)
|
| In vitro |
TAK-875 vertoont krachtige agonistische activiteit en hoge bindingsaffiniteit voor de humane GPR40-receptor met een Ki van 38 nM. TAK-875 vertoont een zwakkere affiniteit voor de rat GPR40-receptor met een Ki van 140 nM. TAK-875 vertoont uitstekende selectiviteit, aangezien TAK-875 weinig agonistische potentie heeft ten opzichte van andere leden van de FFA-receptorfamilie met een EC50 van >10 μM. TAK-875-behandeling induceert een concentratieafhankelijke toename van de intracellulaire IP-productie in CHO-hGPR40 met een EC50 van 72 nM, krachtiger dan die van de endogene ligandagonist oliezuur, die veel hogere ligandconcentraties vereist om de receptor te activeren met een EC50 van 29,9 μM. Noch TAK-875, noch oliezuur lokt een IP-respons uit in controle CHO-cellen zonder hGPR40. In overeenstemming met de activering van de Gqα-gemedieerde signaalroute, verhoogt TAK-875 de glucoseafhankelijke insulinesecretie in pancreas-β-cellen. Langdurige stimulatie van GPR40/FFA1 door TAK-875 veroorzaakt geen pancreas-β-celdysfunctie of inductie van apoptose. |
| In vivo |
In een ratmodel van diabetes vermindert een enkele orale dosis TAK-875 van 0,3-3 mg/kg de bloedglucose-excursie en verhoogt het de insulinesecretie tijdens een orale glucosetolerantietest, wanneer TAK-875 1 uur vóór een orale glucosechallenge wordt toegediend. Bij type 2 diabetische N-STZ-1.5 ratten vertoont de toediening van TAK-875 (1-10 mg/kg p.o.) een duidelijke verbetering in glucosetolerantie en verhoogt het de insulinesecretie. Bovendien verhoogt TAK-875 (10 mg/kg, p.o.) significant de plasma-insulinewaarden en vermindert het nuchtere hyperglycemie bij mannelijke Zucker-diabetische vetratten, terwijl bij nuchtere normale Sprague-Dawley-ratten TAK-875 noch de insulinesecretie verhoogt, noch hypoglycemie veroorzaakt, zelfs bij 30 mg/kg. |
Referenties |
|
Informatie over klinische proeven
(gegevens van https://clinicaltrials.gov, bijgewerkt op 2024-05-22)
| NCT-nummer | Werving | Aandoeningen | Sponsor/medewerkers | Startdatum | Fasen |
|---|---|---|---|---|---|
| NCT01496443 | Completed | Pharmacokinetics |
Takeda |
January 2012 | Phase 1 |
| NCT00949091 | Completed | Diabetes Mellitus Type 2 |
Takeda |
January 2009 | Phase 1 |
Technische ondersteuning
Tel: +1-832-582-8158 Ext:3
Als u nog andere vragen heeft, laat dan een bericht achter.
