alleen voor onderzoeksdoeleinden
BGJ398 (Infigratinib) FGFR remmer
Cat.nr.S2183
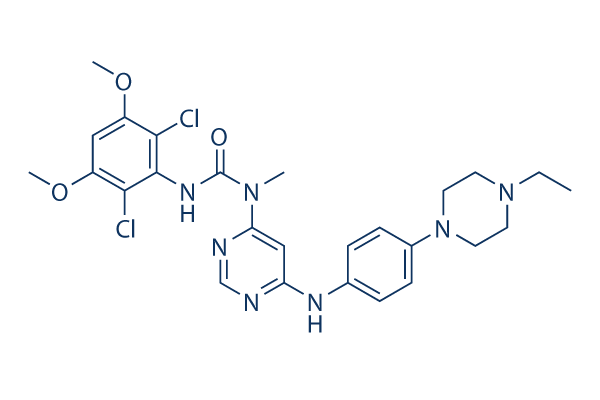
Chemische structuur
Molecuulgewicht: 560.48
Kwaliteitscontrole
Producten die vaak samen worden gebruikt met BGJ398 (Infigratinib)
| Gerelateerde doelwitten | EGFR VEGFR JAK PDGFR Src HIF FLT FLT3 HER2 Bcr-Abl |
|---|---|
| Overig FGFR Inhibitoren | PD173074 AZD4547 (Fexagratinib) BLU9931 Futibatinib (TAS-120) LY2874455 PD-166866 Zoligratinib (Debio-1347) H3B-6527 Fisogatinib (BLU-554) SSR128129E |
Celkweek, behandeling & werkzame concentratie
| Cellijnen | Assaytype | Concentratie | Incubatietijd | Formulering | Activiteitsbeschrijving | PMID |
|---|---|---|---|---|---|---|
| HCC | Growth Inhibition Assay | 1-2500 nM | 48 h | IC50= 2359 nm | 25688743 | |
| HCC | Growth Inhibition Assay | 1-2500 nM | 48 h | IC50=1124 nm | 25688743 | |
| HCT116 | Growth Inhibition Assay | 48 h | IC50=3 μM | 24503538 | ||
| HKH2 | Growth Inhibition Assay | 48 h | IC50=4 μM | 24503538 | ||
| RKO | Growth Inhibition Assay | 48 h | IC50=1.2 μM | 24503538 | ||
| LS174T | Growth Inhibition Assay | 48 h | IC50=4 μM | 24503538 | ||
| HCD9 | Growth Inhibition Assay | 0.5-5 μM | 48/72 h | DMSO | decreases cell viability | 24135816 |
| HCT116 | Growth Inhibition Assay | 0.5-5 μM | 48/72 h | DMSO | decreases cell viability | 24135816 |
| SNU-C1 | Growth Inhibition Assay | 0.5-5 μM | 48/72 h | DMSO | no effect | 24135816 |
| MFE280 | Growth Inhibition Assay | IC50=2.63 ± 0.82 μM | 23443805 | |||
| AN3CA | Growth Inhibition Assay | IC50=1.00 ± 0.20 μM | 23443805 | |||
| HEC155 | Growth Inhibition Assay | IC50=4.74 ± 1.09 μM | 23443805 | |||
| MFE296 | Growth Inhibition Assay | IC50=2.86 ± 0.20 μM | 23443805 | |||
| SPAC1S | Growth Inhibition Assay | IC50=3.19 ± 0.93 μM | 23443805 | |||
| RL952 | Growth Inhibition Assay | IC50=3.41 ± 0.23 μM | 23443805 | |||
| EN1 | Growth Inhibition Assay | IC50=4.75 ± 0.62 μM | 23443805 | |||
| SNGII | Growth Inhibition Assay | IC50=4.29 ± 0.58 μM | 23443805 | |||
| ISHIKAWA | Growth Inhibition Assay | IC50=5.48 ± 0.03 μM | 23443805 | |||
| HEC1A | Growth Inhibition Assay | IC50=10.00 ± 1.00 μM | 23443805 | |||
| KLE | Growth Inhibition Assay | IC50=3.03 ± 0.11 μM | 23443805 | |||
| SNGM | Growth Inhibition Assay | IC50=5.00 ± 0.41 μM | 23443805 | |||
| USPC2 | Growth Inhibition Assay | IC50=7.00 ± 0.21 μM | 23443805 | |||
| EN | Growth Inhibition Assay | IC50=6.03 ± 0.31 μM | 23443805 | |||
| MFE319 | Growth Inhibition Assay | IC50=5.37 ± 0.03 μM | 23443805 | |||
| EFE184 | Growth Inhibition Assay | IC50=8.04 ± 0.69 μM | 23443805 | |||
| ECC1 | Growth Inhibition Assay | IC50=6.74 ± 0.59 μM | 23443805 | |||
| HEC1B | Growth Inhibition Assay | IC50=6.45 ± 0.67 μM | 23443805 | |||
| USPC1 | Growth Inhibition Assay | IC50=5.75 ± 0.50 μM | 23443805 | |||
| SPAC1L | Growth Inhibition Assay | IC50=4.92 ± 0.50 μM | 23443805 | |||
| HCC827 | Function assay | Displacement of [3H]-cyclopamine from SMO V404M mutant in gefitinib resistant human HCC827 cells by scintillation counting, Ki = 0.0465 μM. | 28787156 | |||
| SJ-GBM2 | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for SJ-GBM2 cells | 29435139 | |||
| NB-EBc1 | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for NB-EBc1 cells | 29435139 | |||
| sf9 | Function assay | 60 mins | Inhibition of non-phosphorylated N-terminal His6-tagged FGFR4 C552A mutant (G442 to E753 residues) (unknown origin) expressed in sf9 cells using 5-Fluo-Ahx-KKKKEEIYFFFG-NH2 as substrate after 60 mins by microfluidic mobility shift assay, IC50 = 0.00082 μM. | ChEMBL | ||
| sf9 | Function assay | 60 mins | Inhibition of wild type non-phosphorylated N-terminal His6-tagged FGFR4 (G442 to E753 residues) (unknown origin) expressed in sf9 cells using 5-Fluo-Ahx-KKKKEEIYFFFG-NH2 as substrate after 60 mins by microfluidic mobility shift assay, IC50 = 0.062 μM. | ChEMBL | ||
| sf9 | Function assay | 60 mins | Inhibition of non-phosphorylated N-terminal His6-tagged FGFR4 C477A mutant (G442 to E753 residues) (unknown origin) expressed in sf9 cells using 5-Fluo-Ahx-KKKKEEIYFFFG-NH2 as substrate after 60 mins by microfluidic mobility shift assay, IC50 = 0.064 μM. | ChEMBL | ||
| Klik om meer experimentele gegevens over cellijnen te bekijken | ||||||
Chemische informatie, opslag en stabiliteit
| Molecuulgewicht | 560.48 | Formule | C26H31Cl2N7O3 |
Opslag (vanaf de datum van ontvangst) | |
|---|---|---|---|---|---|
| CAS-nr. | 872511-34-7 | SDF downloaden | Opslag van stamoplossingen |
|
|
| Synoniemen | NVP-BGJ398 | Smiles | CCN1CCN(CC1)C2=CC=C(C=C2)NC3=CC(=NC=N3)N(C)C(=O)NC4=C(C(=CC(=C4Cl)OC)OC)Cl | ||
Oplosbaarheid
|
In vitro |
DMSO
: 3 mg/mL
(5.35 mM)
Water : Insoluble Ethanol : Insoluble |
Molariteitscalculator
|
In vivo |
|||||
In vivo formulatiecalculator (heldere oplossing)
Stap 1: Voer onderstaande informatie in (Aanbevolen: een extra dier om rekening te houden met verlies tijdens het experiment)
Stap 2: Voer de in vivo formulering in (Dit is alleen de calculator, geen formulering. Neem eerst contact met ons op als er geen in vivo formulering is in de sectie oplosbaarheid.)
Berekeningsresultaten:
Werkconcentratie: mg/ml;
Methode voor het bereiden van DMSO-moedervloeistof: mg geneesmiddel vooropgelost in μL DMSO ( Concentratie moedervloeistof mg/mL, Neem eerst contact met ons op als de concentratie de DMSO-oplosbaarheid van de batch van het geneesmiddel overschrijdt. )
Methode voor het bereiden van in vivo formulering: Neem μL DMSO moedervloeistof, voeg daarna toeμL PEG300, mengen en verhelderen, daarna toevoegenμL Tween 80, mengen en verhelderen, daarna toevoegen μL ddH2O, mengen en verhelderen.
Methode voor het bereiden van in vivo formulering: Neem μL DMSO moedervloeistof, voeg daarna toe μL Maïsolie, mengen en verhelderen.
Opmerking: 1. Zorg ervoor dat de vloeistof helder is voordat u het volgende oplosmiddel toevoegt.
2. Zorg ervoor dat u het/de oplosmiddel(en) in de juiste volgorde toevoegt. U moet ervoor zorgen dat de verkregen oplossing, bij de vorige toevoeging, een heldere oplossing is voordat u verdergaat met het toevoegen van het volgende oplosmiddel. Fysieke methoden zoals vortexen, ultrasoon of een warmwaterbad kunnen worden gebruikt om het oplossen te bevorderen.
Werkingsmechanisme
| Targets/IC50/Ki |
FGFR1
(Cell-free assay) 0.9 nM
FGFR3
(Cell-free assay) 1.0 nM
FGFR2
(Cell-free assay) 1.4 nM
FGFR3 (K650E)
(Cell-free assay) 4.9 nM
FGFR4
(Cell-free assay) 60 nM
|
|---|---|
| In vitro |
Infigratinib (BGJ398) voorkomt ook VEGFR2 met lage potentie, met een IC50 van 0,18 μM voor het remmen van dit doelwit. Het onderdrukt andere kinasen, waaronder ABL, FYN, KIT, LCK, LYN en YES met IC50-waarden van respectievelijk 2,3 μM, 1,9 μM, 0,75 μM, 2,5 μM, 0,3 μM en 1,1 μM. Op cellulair niveau remt deze verbinding de proliferatie van de FGFR1-, FGFR2-Q- en FGFR3-afhankelijke BaF3-cellen met een IC50 van respectievelijk 2,9 μM, 2,0 μM en 2 μM. Het interfereert met autofosforylering op specifieke tyrosineresiduen, waaronder FGFR-WT, FGFR2-WT, FGFR3-K650E, FGFR3-S249C en FGFR4-WT met een IC50 van respectievelijk 4,6 nM, 4,9 nM, 5 nM, 5 nM en 168 nM. Bovendien onderdrukt het de proliferatie van kankercellen met wildtype (WT) FGFR3-overexpressie, zoals RT112, RT4, SW780 en JMSU1, met een IC50 van respectievelijk 5 nM, 30 nM, 32 nM en 15 nM.
|
| Kinase Assay |
Radiometrische kinase-assay
|
|
De enzymatische kinaseactiviteit wordt beoordeeld door de fosforylering van een synthetisch substraat te meten door het gezuiverde GST-fusie FGFR3-K650E kinase-domein, in aanwezigheid van radiogemerkt ATP. Enzymactiviteiten worden gemeten door 10 μL van een 3-voudig geconcentreerde oplossing van Infigratinib (BGJ398) of controle te mengen met 10 μL van het corresponderende substraatmengsel (peptidisch substraat, ATP en [γ33P]ATP). De reacties worden geïnitieerd door toevoeging van 10 μL van een 3-voudig geconcentreerde oplossing van het enzym in assaybuffer. De uiteindelijke concentraties van de assaycomponenten zijn als volgt: 10 ng GST-FGFR3-K650E, 20 mM Tris-HCl, pH 7,5, 3 mM MnCl2, 3 mM MgCl2, 1 mM DTT, 250 μg/mL PEG 20000, 2 μg/mL poly(EY) 4:1, 1% DMSO en 0,5 μM ATP (γ-[33P]-ATP 0,1 μCi). De assay wordt uitgevoerd volgens de filterbindings (FB) methode in 96-well platen bij kamertemperatuur gedurende 10 minuten in een eindvolume van 30 μL inclusief deze verbinding. De enzymatische reacties worden gestopt door de toevoeging van 20 μL 125 mM EDTA, en de incorporatie van 33P in de polypeptidische substraten wordt gekwantificeerd als volgt: 30 μL van het gestopte reactiemengsel wordt overgebracht op Immobilon-PVDF membranen die vooraf 5 minuten met methanol waren geweekt, met water gespoeld, 5 minuten met 0,5% H3PO4 waren geweekt en op een vacuümverdeelstuk met ontkoppelde vacuümbron waren gemonteerd. Na het spotten wordt vacuüm aangesloten en wordt elke put gespoeld met 0,5% H3PO4 (200 μL). Vrije membranen worden verwijderd en vier keer gewassen op een schudapparaat met 1% H3PO4 en eenmaal met ethanol. Membranen worden gedroogd en bedekt met toevoeging van 10 μL/put van een scintillatievloeistof. De platen worden uiteindelijk verzegeld en geteld in een microplaatscintillatieteller. IC50-waarden worden berekend door lineaire regressieanalyse van het percentage remming.
|
|
| In vivo |
In dit orthotopische xenograftblaaskankermodel induceert BGJ398 tumorggroeiremming en stasis na orale toediening gedurende 12 opeenvolgende dagen in doses van respectievelijk 10 en 30 mg/kg. Interessant is dat de dieren die deze verbinding kregen, ofwel geen gewichtsverlies (10 mg/kg) of 10% gewichtstoename (30 mg/kg) vertoonden, een verdere indicatie van werkzaamheid. RT112-tumor dragende en vrouwelijke Rowett-ratten krijgen een enkele orale toediening van het monofosfaatzout van Infigratinib (BGJ398) in doses van 4,25 en 8,51 mg/kg. Het verlaagt de niveaus van pFRS2 en pMAPK significant op een dosisafhankelijke manier. Bovendien remt het significant bFGF-gestimuleerde Angiogenesis op een dosisafhankelijke manier. Het beïnvloedt echter de VEGF-geïnduceerde bloedvatvorming niet.
|
Referenties |
Toepassingen
| Methoden | Biomarkers | Afbeeldingen | PMID |
|---|---|---|---|
| Western blot | pFGFR1 / FGFR1 / pFRS2 / FRS2 / MEK / ERK p-YAP (S127) / YAP Mcl-1 Cyclin D1 / Cyclin A / Cyclin B / γ-H2AX / Cleaved caspase-9 / PARP Snail / Slug / ZEB1 p-FRS2 / FRS2 / p-AKT / AKT / p-ERK / ERK |
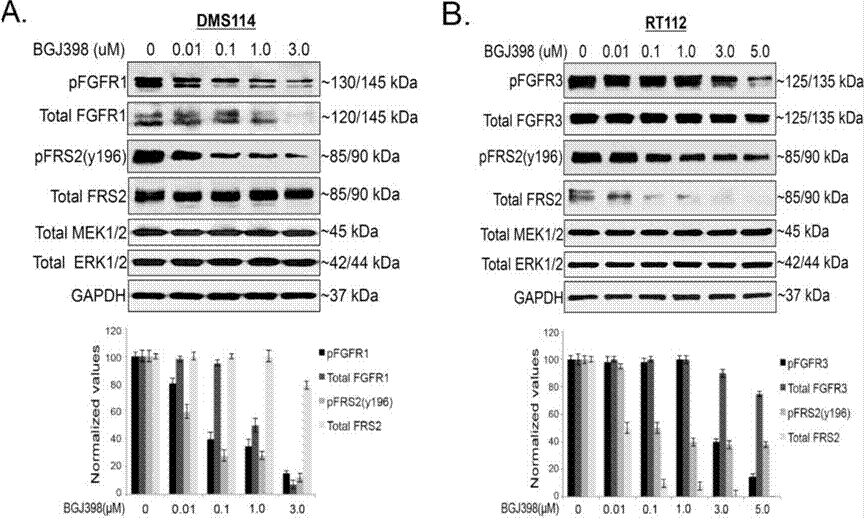
|
28255027 |
| Immunofluorescence | YAP |
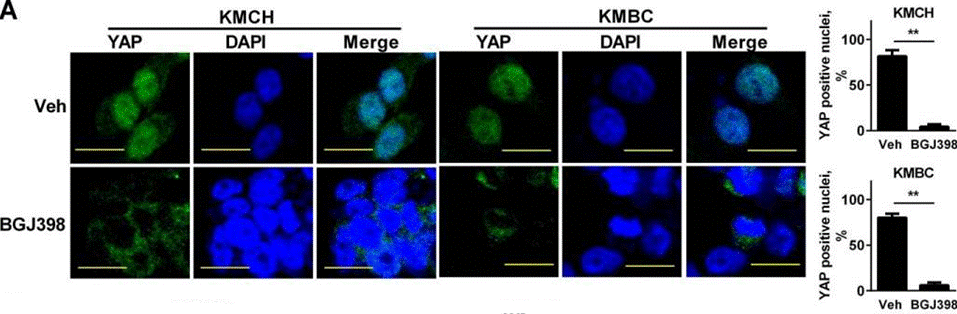
|
26826125 |
| Growth inhibition assay | Cell viability IC50 |
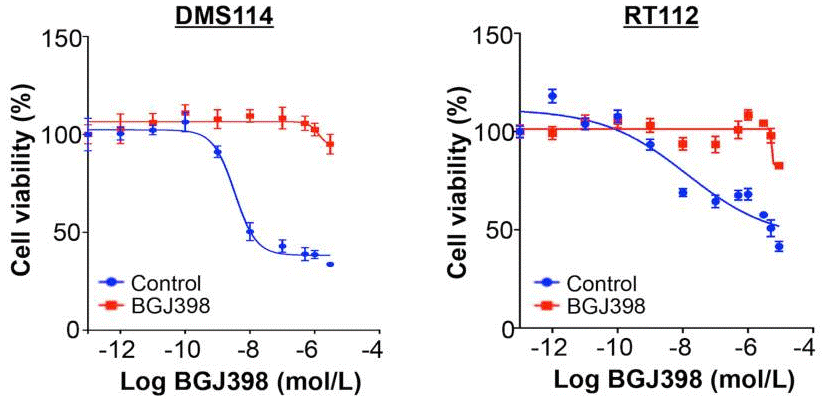
|
28255027 |
Informatie over klinische proeven
(gegevens van https://clinicaltrials.gov, bijgewerkt op 2024-05-22)
| NCT-nummer | Werving | Aandoeningen | Sponsor/medewerkers | Startdatum | Fasen |
|---|---|---|---|---|---|
| NCT03510455 | Terminated | Tumor-Induced Osteomalacia|Oncogenic Osteomalacia |
National Institute of Dental and Craniofacial Research (NIDCR)|National Institutes of Health Clinical Center (CC) |
February 27 2019 | Phase 2 |
| NCT02312804 | Withdrawn | Cancer of Cervix|Tumors |
The University of Texas Health Science Center at San Antonio |
January 2015 | Phase 1 |
| NCT02160041 | Terminated | Solid Tumor|Hematologic Malignancies |
Novartis Pharmaceuticals|Novartis |
July 24 2014 | Phase 2 |
| NCT01928459 | Completed | Advanced Solid Tumors|Metastatic Solid Tumors |
Novartis Pharmaceuticals|Novartis |
October 2013 | Phase 1 |
| NCT01004224 | Completed | Advanced Solid Tumors With Alterations of FGFR1 2 and or 3|Squamous Lung Cancer With FGFR1 Amplification|Bladder Cancer With FGFR3 Mutation or Fusion|Advanced Solid Tumors With FGFR1 Amplication|Advanced Solid Tumors With FGFR2 Amplication|Advanced Solid Tumors With FGFR3 Mutation |
Novartis Pharmaceuticals|Novartis |
December 11 2009 | Phase 1 |
Technische ondersteuning
Tel: +1-832-582-8158 Ext:3
Als u nog andere vragen heeft, laat dan een bericht achter.
Veelgestelde vragen
Vraag 1:
If you have any suggestions about the formulation of this compound for a direct oral gavage administration?
Antwoord:
It can be dissolved in 30% PEG400/0.5% Tween80/5% Propylene glycol at 30 mg/ml as a suspension.
