alleen voor onderzoeksdoeleinden
OSI-930 c-Kit remmer
Cat.nr.S1220
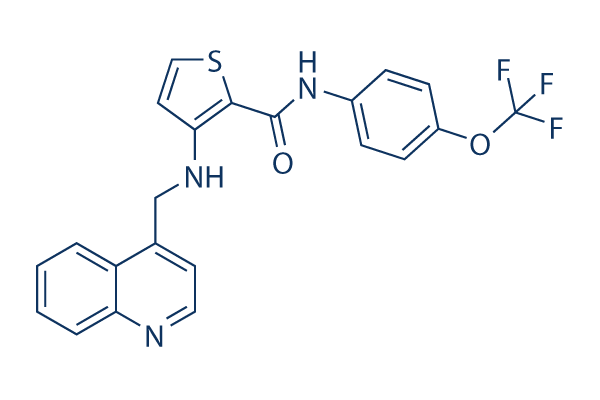
Chemische structuur
Molecuulgewicht: 443.44
Kwaliteitscontrole
| Gerelateerde doelwitten | EGFR VEGFR PDGFR FGFR c-Met Src MEK CSF-1R FLT3 HER2 |
|---|---|
| Overig c-Kit Inhibitoren | Masitinib Amuvatinib (MP-470) Sitravatinib (MGCD516) PDGFR inhibitor 1 ISCK03 AZD3229 Masitinib mesylate Bezuclastinib Elenestinib phosphate M4205(IDRX-42) |
Chemische informatie, opslag en stabiliteit
| Molecuulgewicht | 443.44 | Formule | C22H16F3N3O2S |
Opslag (vanaf de datum van ontvangst) | |
|---|---|---|---|---|---|
| CAS-nr. | 728033-96-3 | SDF downloaden | Opslag van stamoplossingen |
|
|
| Synoniemen | N/A | Smiles | C1=CC=C2C(=C1)C(=CC=N2)CNC3=C(SC=C3)C(=O)NC4=CC=C(C=C4)OC(F)(F)F | ||
Oplosbaarheid
|
In vitro |
DMSO
: 89 mg/mL
(200.7 mM)
Ethanol : 3 mg/mL Water : Insoluble |
Molariteitscalculator
|
In vivo |
|||||
In vivo formulatiecalculator (heldere oplossing)
Stap 1: Voer onderstaande informatie in (Aanbevolen: een extra dier om rekening te houden met verlies tijdens het experiment)
Stap 2: Voer de in vivo formulering in (Dit is alleen de calculator, geen formulering. Neem eerst contact met ons op als er geen in vivo formulering is in de sectie oplosbaarheid.)
Berekeningsresultaten:
Werkconcentratie: mg/ml;
Methode voor het bereiden van DMSO-moedervloeistof: mg geneesmiddel vooropgelost in μL DMSO ( Concentratie moedervloeistof mg/mL, Neem eerst contact met ons op als de concentratie de DMSO-oplosbaarheid van de batch van het geneesmiddel overschrijdt. )
Methode voor het bereiden van in vivo formulering: Neem μL DMSO moedervloeistof, voeg daarna toeμL PEG300, mengen en verhelderen, daarna toevoegenμL Tween 80, mengen en verhelderen, daarna toevoegen μL ddH2O, mengen en verhelderen.
Methode voor het bereiden van in vivo formulering: Neem μL DMSO moedervloeistof, voeg daarna toe μL Maïsolie, mengen en verhelderen.
Opmerking: 1. Zorg ervoor dat de vloeistof helder is voordat u het volgende oplosmiddel toevoegt.
2. Zorg ervoor dat u het/de oplosmiddel(en) in de juiste volgorde toevoegt. U moet ervoor zorgen dat de verkregen oplossing, bij de vorige toevoeging, een heldere oplossing is voordat u verdergaat met het toevoegen van het volgende oplosmiddel. Fysieke methoden zoals vortexen, ultrasoon of een warmwaterbad kunnen worden gebruikt om het oplossen te bevorderen.
Werkingsmechanisme
| Targets/IC50/Ki |
FLT1
(Cell-free assay) 8 nM
KDR
(Cell-free assay) 9 nM
CSF-1R
(Cell-free assay) 15 nM
LCK
(Cell-free assay) 22 nM
C-Raf
(Cell-free assay) 41 nM
Kit
(Cell-free assay) 80 nM
|
|---|---|
| In vitro |
OSI-930 remt de celproliferatie in de HMC-1 cellijn met een IC50 van 14 nM zonder significant effect op de groei van de COLO-205 cellijn die geen constitutief actieve mutante receptor tyrosine kinase tot expressie brengt. Bovendien induceert deze verbinding ook apoptose in de HMC-1 cellijn met een EC50 van 34 nM. Een recente studie toont aan dat deze chemische stof gezuiverd, recombinant cytochroom P450 (P450) 3A4 inactiveert met een Ki van 24 μM op een tijd- en concentratieafhankelijke manier.
|
| Kinase Assay |
Proteïnekinase-assays
|
|
Proteïnekinase-assays worden intern uitgevoerd met behulp van ELISA-gebaseerde assaymethoden (Kit, KDR, PDGFRα en PDGFRβ) of met een radiometrische methode. Interne ELISA-assays gebruikten poly(Glu:Tyr) als substraat gebonden aan het oppervlak van 96-wells assayplaten; fosforylering wordt vervolgens gedetecteerd met behulp van een antifosfotyrosine-antilichaam geconjugeerd aan HRP. Het gebonden antilichaam wordt vervolgens gekwantificeerd met behulp van ABTS als het peroxidase-substraat door de absorptie bij 405/490 nm te meten. Alle assays gebruiken gezuiverde recombinante kinase-katalytische domeinen die worden uitgedrukt in insectencellen of in bacteriën. Het Kit- en EGFR-eiwit dat wordt gebruikt voor interne assays wordt intern bereid; andere enzymen worden verkregen. Recombinant Kit-eiwit wordt uitgedrukt als een NH2-terminaal glutathion S-transferase fusie-eiwit in insectencellen en wordt aanvankelijk gezuiverd als een niet-gefosforyleerd (niet-geactiveerd) enzym met een relatief hoge Km voor ATP (400 μM). In sommige assays wordt een geactiveerde (tyrosine-gefosforyleerde) vorm van het enzym bereid door incubatie met 1 mM ATP gedurende 1 uur bij 30 °C. Het gefosforyleerde eiwit wordt vervolgens door een ontzoutingskolom geleid om het grootste deel van het ATP te verwijderen en opgeslagen bij -80 °C in buffer die 50% glycerol bevat. De resulterende bereiding heeft een aanzienlijk hogere specifieke activiteit en een lagere Km voor ATP (25 μM) dan de initiële niet-gefosforyleerde bereiding. De remming van Kit-autofosforylering door deze verbinding wordt geanalyseerd door incubatie van het niet-gefosforyleerde enzym bij 30 °C in aanwezigheid van 200 μM ATP en verschillende concentraties van deze chemische stof. De reactie wordt gestopt door aliquotten te verwijderen in SDS-PAGE sample buffer, gevolgd door verwarming tot 100 °C gedurende 5 minuten. De mate van fosforylering van Kit wordt vervolgens bepaald door immunoblotting voor zowel totale Kit als gefosforyleerde Kit.
|
|
| In vivo |
OSI-930, toegediend in de maximaal werkzame dosis van 200 mg/kg via orale gavage, vertoont krachtige antitumoractiviteit in een breed scala aan preklinische xenograftmodellen, waaronder HMC-1, NCI-SNU-5, COLO-205 en U251 xenograftmodellen.
|
Referenties |
|
Informatie over klinische proeven
(gegevens van https://clinicaltrials.gov, bijgewerkt op 2024-05-22)
| NCT-nummer | Werving | Aandoeningen | Sponsor/medewerkers | Startdatum | Fasen |
|---|---|---|---|---|---|
| NCT00513851 | Completed | Advanced Solid Tumors |
Astellas Pharma Inc|OSI Pharmaceuticals |
April 2006 | Phase 1 |
Technische ondersteuning
Tel: +1-832-582-8158 Ext:3
Als u nog andere vragen heeft, laat dan een bericht achter.
