alleen voor onderzoeksdoeleinden
Torcetrapib CETP remmer
Cat.nr.S2792
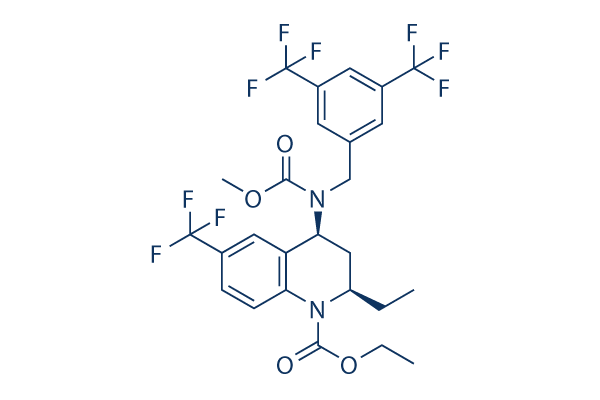
Chemische structuur
Molecuulgewicht: 600.47
Kwaliteitscontrole
| Gerelateerde doelwitten | Dehydrogenase HSP Transferase P450 (e.g. CYP17) PDE phosphatase PPAR Vitamin Carbohydrate Metabolism Mitochondrial Metabolism |
|---|---|
| Overig CETP Inhibitoren | Anacetrapib (MK-0859) Dalcetrapib (JTT-705) Evacetrapib (LY2484595) Obicetrapib |
Chemische informatie, opslag en stabiliteit
| Molecuulgewicht | 600.47 | Formule | C26H25F9N2O4 |
Opslag (vanaf de datum van ontvangst) | |
|---|---|---|---|---|---|
| CAS-nr. | 262352-17-0 | SDF downloaden | Opslag van stamoplossingen |
|
|
| Synoniemen | CP-529414 | Smiles | CCC1CC(C2=C(N1C(=O)OCC)C=CC(=C2)C(F)(F)F)N(CC3=CC(=CC(=C3)C(F)(F)F)C(F)(F)F)C(=O)OC | ||
Oplosbaarheid
|
In vitro |
DMSO
: 120 mg/mL
(199.84 mM)
Ethanol : 6 mg/mL Water : Insoluble |
Molariteitscalculator
|
In vivo |
|||||
In vivo formulatiecalculator (heldere oplossing)
Stap 1: Voer onderstaande informatie in (Aanbevolen: een extra dier om rekening te houden met verlies tijdens het experiment)
Stap 2: Voer de in vivo formulering in (Dit is alleen de calculator, geen formulering. Neem eerst contact met ons op als er geen in vivo formulering is in de sectie oplosbaarheid.)
Berekeningsresultaten:
Werkconcentratie: mg/ml;
Methode voor het bereiden van DMSO-moedervloeistof: mg geneesmiddel vooropgelost in μL DMSO ( Concentratie moedervloeistof mg/mL, Neem eerst contact met ons op als de concentratie de DMSO-oplosbaarheid van de batch van het geneesmiddel overschrijdt. )
Methode voor het bereiden van in vivo formulering: Neem μL DMSO moedervloeistof, voeg daarna toeμL PEG300, mengen en verhelderen, daarna toevoegenμL Tween 80, mengen en verhelderen, daarna toevoegen μL ddH2O, mengen en verhelderen.
Methode voor het bereiden van in vivo formulering: Neem μL DMSO moedervloeistof, voeg daarna toe μL Maïsolie, mengen en verhelderen.
Opmerking: 1. Zorg ervoor dat de vloeistof helder is voordat u het volgende oplosmiddel toevoegt.
2. Zorg ervoor dat u het/de oplosmiddel(en) in de juiste volgorde toevoegt. U moet ervoor zorgen dat de verkregen oplossing, bij de vorige toevoeging, een heldere oplossing is voordat u verdergaat met het toevoegen van het volgende oplosmiddel. Fysieke methoden zoals vortexen, ultrasoon of een warmwaterbad kunnen worden gebruikt om het oplossen te bevorderen.
Werkingsmechanisme
| Targets/IC50/Ki |
CETP
37 nM
|
|---|---|
| In vitro |
Torcetrapib verhoogt dosisafhankelijk de aldosteronafgifte uit H295R-cellen na 24 of 48 uur behandeling met een EC50 van ongeveer 80 nM; dit effect wordt gemedieerd door calciumkanalen, aangezien calciumkanaalblokkers de door deze verbinding geïnduceerde corticosteroïdafgifte en calciumtoename volledig blokkeren. Deze chemische stof (1 μM) verhoogt significant de expressie van de steroïdogene genen CYP11B2 en CYP11B1 in H295R-cellijnen.
|
| In vivo |
Torcetrapib (< 100 mg, dagelijks) verandert de plasmaverdeling van CETP, aangezien het schijnbare molecuulgewicht van de CETP 2 uur na de dosis bij gezonde jonge proefpersonen is verschoven naar een grotere vorm. Deze verbinding behandeling met 10 mg, 30 mg, 60 mg en 120 mg dagelijks en 120 mg tweemaal daags resulteert in respectievelijk 16%, 28%, 62%, 73% en 91% toenames in plasma HDL-C, zonder significante veranderingen in TPC bij gezonde jonge proefpersonen. Het resulteert in een toename van 72,1% in high-density lipoproteïne cholesterol en een afname van 24,9% in low-density lipoproteïne cholesterol, naast een toename van 5,4 mm Hg in systolische bloeddruk, een afname van serumkalium en toenames van serumnatrium, bicarbonaat en aldosteron, bij patiënten met een hoog cardiovasculair risico na 12 maanden behandeling. Dit middel verhoogt de HDL-cholesterolspiegels met 50% en 60% bij een dosis van respectievelijk 60 mg dagelijks en 120 mg dagelijks, zowel bij gezonde als matig hyperlipidemische proefpersonen. 60 mg dagelijks verhoogt de HDL-gemedieerde netto cholesterol-efflux uit schuimcellen voornamelijk door verhoging van de HDL-concentraties, terwijl 120 mg dagelijks van deze verbinding de cholesterol-efflux verhoogt door zowel de HDL-concentratie te verhogen als door een verhoogde efflux te veroorzaken bij overeenkomstige HDL-concentraties. Deze chemische stof (90 mg/kg/dag) resulteert in een 70% remming van CE-overdracht bij konijnen die een atherogeen dieet kregen. Het (90 mg/kg/dag) verhoogt de gemiddelde HDL-C-spiegels met meer dan 3-voudig en de apoA-I-spiegels met 2,5-voudig in plasma bij konijnen die een atherogeen dieet kregen. Het behandelde dier heeft een meervoudige toename in HDL-C AUC en een corresponderende vermindering in aortalesiegebied met 60% vermindering van aorta-vrij cholesterol (FC) en cholesterylester (EC) bij konijnen die een atherogeen dieet kregen. Sera van met deze verbinding behandelde konijnen stimuleren de vrije cholesterol-efflux in significant grotere mate dan sera van controlekonijnen.
|
Referenties |
|
Informatie over klinische proeven
(gegevens van https://clinicaltrials.gov, bijgewerkt op 2024-05-22)
| NCT-nummer | Werving | Aandoeningen | Sponsor/medewerkers | Startdatum | Fasen |
|---|---|---|---|---|---|
| NCT00139061 | Completed | Hyperlipidemia |
Pfizer |
March 2005 | Phase 3 |
Technische ondersteuning
Tel: +1-832-582-8158 Ext:3
Als u nog andere vragen heeft, laat dan een bericht achter.
