alleen voor onderzoeksdoeleinden
Telbivudine Reverse Transcriptase remmer
Cat.nr.S1651
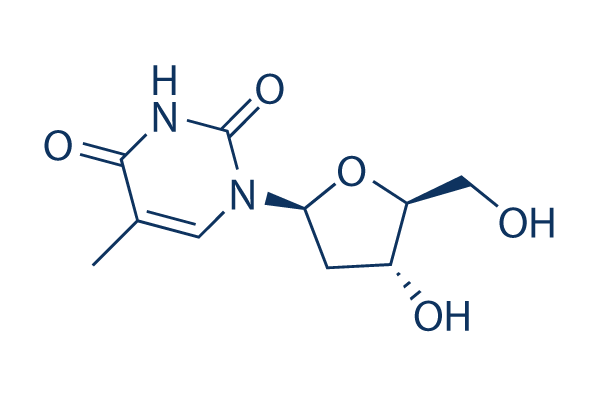
Chemische structuur
Molecuulgewicht: 242.23
Kwaliteitscontrole
| Gerelateerde doelwitten | Integrase Bacterial Antibiotics Anti-infection Fungal Antiviral COVID-19 Parasite HIV HCV Protease |
|---|---|
| Overig Reverse Transcriptase Inhibitoren | Dapivirine (TMC120) Fangchinoline Salicylanilide 3'-Fluoro-3'-deoxythymidine (Alovudine) Ulonivirine Lersivirine (UK-453061) Bifendate 4-Chloro-2-(trifluoroacetyl)aniline hydrochloride |
Chemische informatie, opslag en stabiliteit
| Molecuulgewicht | 242.23 | Formule | C10H14N2O5 |
Opslag (vanaf de datum van ontvangst) | |
|---|---|---|---|---|---|
| CAS-nr. | 3424-98-4 | SDF downloaden | Opslag van stamoplossingen |
|
|
| Synoniemen | NV 02B | Smiles | CC1=CN(C(=O)NC1=O)C2CC(C(O2)CO)O | ||
Oplosbaarheid
|
In vitro |
DMSO
: 48 mg/mL
(198.15 mM)
Water : 48 mg/mL Ethanol : 2 mg/mL |
Molariteitscalculator
|
In vivo |
|||||
In vivo formulatiecalculator (heldere oplossing)
Stap 1: Voer onderstaande informatie in (Aanbevolen: een extra dier om rekening te houden met verlies tijdens het experiment)
Stap 2: Voer de in vivo formulering in (Dit is alleen de calculator, geen formulering. Neem eerst contact met ons op als er geen in vivo formulering is in de sectie oplosbaarheid.)
Berekeningsresultaten:
Werkconcentratie: mg/ml;
Methode voor het bereiden van DMSO-moedervloeistof: mg geneesmiddel vooropgelost in μL DMSO ( Concentratie moedervloeistof mg/mL, Neem eerst contact met ons op als de concentratie de DMSO-oplosbaarheid van de batch van het geneesmiddel overschrijdt. )
Methode voor het bereiden van in vivo formulering: Neem μL DMSO moedervloeistof, voeg daarna toeμL PEG300, mengen en verhelderen, daarna toevoegenμL Tween 80, mengen en verhelderen, daarna toevoegen μL ddH2O, mengen en verhelderen.
Methode voor het bereiden van in vivo formulering: Neem μL DMSO moedervloeistof, voeg daarna toe μL Maïsolie, mengen en verhelderen.
Opmerking: 1. Zorg ervoor dat de vloeistof helder is voordat u het volgende oplosmiddel toevoegt.
2. Zorg ervoor dat u het/de oplosmiddel(en) in de juiste volgorde toevoegt. U moet ervoor zorgen dat de verkregen oplossing, bij de vorige toevoeging, een heldere oplossing is voordat u verdergaat met het toevoegen van het volgende oplosmiddel. Fysieke methoden zoals vortexen, ultrasoon of een warmwaterbad kunnen worden gebruikt om het oplossen te bevorderen.
Werkingsmechanisme
| Targets/IC50/Ki |
HBV RT
|
|---|---|
| In vitro |
Telbivudine vertoont een potente, selectieve en specifieke antivirale activiteit tegen HBV en andere hepadna-virussen. Deze verbinding wordt gefosforyleerd door intracellulaire thymidinekinases tot de actieve trifosfaatvorm, die een intracellulaire halfwaardetijd van 14 uur heeft. Het 5′-trifosfaat remt HBV DNA-polymerase (reverse transcriptase) door te concurreren met het natuurlijke substraat, dTTP. Deze chemische stof verhoogt significant de productie van tumornecrosefactor-alfa en interleukine-12 in MHV-3-geïnduceerde macrofagen. Het verhoogt significant de serumniveaus van interferon-gamma. Deze behandeling verbetert het vermogen van T-cellen om te prolifereren en cytokinen af te scheiden, maar beïnvloedt de cytotoxiciteit van geïnfecteerde hepatocyten niet. Het onderdrukt de expressie van programmed death ligand 1 op T-cellen. De verbinding blijft actief, zoals blijkt uit respectievelijke vouwveranderingen van 0,5 (N236T) en 1,0 (A181V en A194T). Het is niet actief tegen HBV-stammen met lamivudine-mutaties L180M/M204V/I, maar blijft in vitro actief tegen de M204V-enkele mutant, wat mogelijk het verschil in resistentieprofielen tussen Telbivudine en lamivudine verklaart. |
Referenties |
|
Informatie over klinische proeven
(gegevens van https://clinicaltrials.gov, bijgewerkt op 2024-05-22)
| NCT-nummer | Werving | Aandoeningen | Sponsor/medewerkers | Startdatum | Fasen |
|---|---|---|---|---|---|
| NCT02956850 | Completed | Hepatitis B Chronic |
Hoffmann-La Roche |
December 12 2016 | Phase 1 |
| NCT02894554 | Terminated | HBsAg-positive Renal Allograft Recipients |
National Taiwan University Hospital |
July 2014 | Phase 4 |
| NCT01379508 | Completed | Chronic Hepatitis B |
Novartis Pharmaceuticals|Novartis |
March 21 2011 | Phase 4 |
| NCT01163240 | Completed | Liver Diseases|Hepatitis Chronic|Hepatitis Viral Human|Hepatitis|Virus Diseases|Digestive System Diseases|Hepatitis B Chronic|Hepatitis B|DNA Virus Infections |
Novartis Pharmaceuticals|Novartis |
June 2009 | -- |
| NCT00877149 | Completed | Compensated Chronic Hepatitis B |
Novartis Pharmaceuticals|Novartis |
March 2009 | Phase 4 |
Technische ondersteuning
Tel: +1-832-582-8158 Ext:3
Als u nog andere vragen heeft, laat dan een bericht achter.
