réservé à la recherche
JTC-801 Opioid Receptor antagoniste
N° Cat.S2722
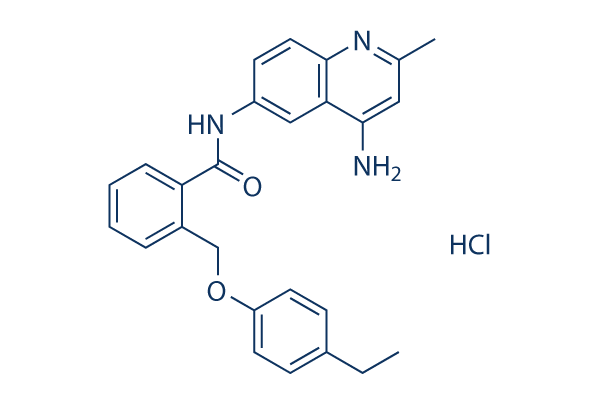
Structure chimique
Poids moléculaire: 447.96
Contrôle qualité
- Cité dans Nature Medicine pour sa qualité supérieure
- COA
- NMR
- SDS
- Fiche technique
| Cibles apparentées | Adrenergic Receptor AChR 5-HT Receptor COX Calcium Channel Histamine Receptor Dopamine Receptor GABA Receptor TRP Channel Cholinesterase (ChE) |
|---|---|
| Autre Opioid Receptor Inhibiteurs | (+)-Matrine Racecadotril Trimebutine Docusate Sodium Trimebutine maleate Asimadoline hydrochloride BMS-986122 Naloxegol Oxalate methylnaltrexone bromide Aticaprant |
Informations chimiques, stockage et stabilité
| Poids moléculaire | 447.96 | Formule | C26H25N3O2.HCl |
Stockage (À partir de la date de réception) | |
|---|---|---|---|---|---|
| N° CAS | 244218-51-7 | Télécharger le SDF | Stockage des solutions mères |
|
|
| Synonymes | N/A | Smiles | CCC1=CC=C(C=C1)OCC2=CC=CC=C2C(=O)NC3=CC4=C(C=C(N=C4C=C3)C)N.Cl | ||
Solubilité
|
In vitro |
DMSO
: 90 mg/mL
(200.91 mM)
Ethanol : 31 mg/mL Water : Insoluble |
Calculateur de molarité
|
In vivo |
|||||
Calculateur de formulation in vivo (Solution claire)
Étape 1 : Entrez les informations ci-dessous (Recommandé : Un animal supplémentaire pour tenir compte des pertes pendant lexpérience)
Étape 2 : Entrez la formulation in vivo (Ceci nest que le calculateur, pas la formulation. Veuillez nous contacter dabord sil ny a pas de formulation in vivo dans la section Solubilité.)
Résultats du calcul :
Concentration de travail : mg/ml;
Méthode de préparation du liquide maître DMSO : mg médicament prédissous dans μL DMSO ( Concentration du liquide maître mg/mL, Veuillez nous contacter dabord si la concentration dépasse la solubilité du DMSO du lot de médicament. )
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, ajouter ensuiteμL PEG300, mélanger et clarifier, ajouter ensuiteμL Tween 80, mélanger et clarifier, ajouter ensuite μL ddH2O, mélanger et clarifier.
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, ajouter ensuite μL Huile de maïs, mélanger et clarifier.
Remarque : 1. Assurez-vous que le liquide est clair avant dajouter le solvant suivant.
2. Assurez-vous dajouter le(s) solvant(s) dans lordre. Vous devez vous assurer que la solution obtenue lors de lajout précédent est une solution claire avant de procéder à lajout du solvant suivant. Des méthodes physiques telles que le vortex, les ultrasons ou le bain-marie peuvent être utilisées pour faciliter la dissolution.
Mécanisme daction
| Targets/IC50/Ki |
Opioid receptor-like1 (ORL1)
94 nM
|
|---|---|
| In vitro |
JTC-801 présente une sélectivité d'environ 12,5, 129 et 1055 fois pour le récepteur ORL1 (Ki = 8,2 nM) par rapport aux récepteurs opioïdes μ, κ et δ, respectivement. Ce composé n'inhibe pas l'accumulation d'AMP cyclique stimulée par la forskoline dans les cellules HeLa exprimant le récepteur ORL1 humain, mais il empêche l'inhibition induite par la nociceptine de l'accumulation d'AMP cyclique, indiquant que cette substance chimique possède une activité antagoniste complète. Dans la membrane cérébrocorticale de rat, ce composé inhibe le récepteur ORL1 avec une IC50 de 472 nM et le récepteur μ avec une IC50 de 1831 nM. Il antagonise complètement la suppression de la nociceptine sur l'accumulation d'AMP cyclique induite par la forskoline avec une IC50 de 2,58 μM dans les cellules HeLa exprimant le récepteur ORL1.
|
| In vivo |
L'administration orale de JTC-801 (0,3-3 mg/kg) antagonise l'allodynie induite par la nociceptine chez la souris, et montre un effet analgésique dans un test de plaque chauffante utilisant des souris et dans un test au formol utilisant des rats. Dans le test de la plaque chauffante chez la souris, ce composé prolonge la latence de la réponse d'évasion (ERL) ou le stimulus thermique exposé avec des doses efficaces minimales (MED) de 0,01 mg/kg par voie i.v. ou de 1 mg/kg par voie orale. Dans le test au formol chez le rat, il réduit les première et deuxième phases de la réponse nociceptive avec des MED de 0,01 mg/kg71 par voie i.v. ou de 1 mg/kg par voie orale. Cette substance chimique normalise la latence de retrait de la patte (PWL) de manière dose-dépendante. Bien qu'elle n'inhibe pas une diminution du contenu minéral osseux (BMC) et de la densité minérale osseuse (BMD) induite par une lésion par constriction chronique (CCI), elle inhibe une augmentation du nombre d'ostéoclastes. L'allodynie tactile induite par la ligature des nerfs spinaux L5/L6 est inversée par l'administration systémique (3-30 mg/kg) et spinale (22,5 et 45 pg) de ce composé de manière dose-dépendante. De plus, le traitement systémique réduit l'immunoréactivité de type Fos dans la corne dorsale de la moelle épinière (laminae I/II). Il produit des effets anti-allodyniques mécaniques et froids dose-dépendants avec une ED50 de 0,83 mg/kg et 1,02 mg/kg, respectivement.
|
Références |
|
Support technique
Tel: +1-832-582-8158 Ext:3
Si vous avez dautres questions, veuillez laisser un message.
