réservé à la recherche
Cabozantinib malate VEGFR inhibiteur
N° Cat.S4001
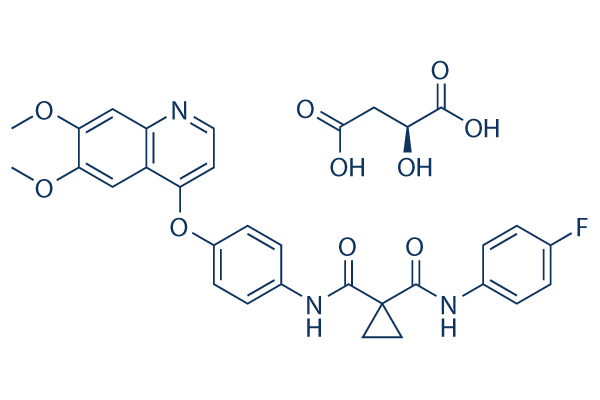
Structure chimique
Poids moléculaire: 635.59
Contrôle qualité
| Cibles apparentées | EGFR PDGFR FGFR c-Met Src MEK CSF-1R FLT3 HER2 c-Kit |
|---|---|
| Autre VEGFR Inhibiteurs | SAR131675 SU 5402 Cediranib (AZD2171) Vatalanib (PTK787) 2HCl Anlotinib (AL3818) Dihydrochloride Linifanib (ABT-869) Apatinib (YN968D1) Apatinib (YN968D1) mesylate Ki8751 ZM 323881 HCl |
Informations chimiques, stockage et stabilité
| Poids moléculaire | 635.59 | Formule | C28H24FN3O5.C4H6O5 |
Stockage (À partir de la date de réception) | |
|---|---|---|---|---|---|
| N° CAS | 1140909-48-3 | Télécharger le SDF | Stockage des solutions mères |
|
|
| Synonymes | XL184 | Smiles | COC1=CC2=C(C=CN=C2C=C1OC)OC3=CC=C(C=C3)NC(=O)C4(CC4)C(=O)NC5=CC=C(C=C5)F.C(C(C(=O)O)O)C(=O)O | ||
Solubilité
|
In vitro |
DMSO
: 100 mg/mL
(157.33 mM)
Water : Insoluble Ethanol : Insoluble |
Calculateur de molarité
|
In vivo |
|||||
Calculateur de formulation in vivo (Solution claire)
Étape 1 : Entrez les informations ci-dessous (Recommandé : Un animal supplémentaire pour tenir compte des pertes pendant lexpérience)
Étape 2 : Entrez la formulation in vivo (Ceci nest que le calculateur, pas la formulation. Veuillez nous contacter dabord sil ny a pas de formulation in vivo dans la section Solubilité.)
Résultats du calcul :
Concentration de travail : mg/ml;
Méthode de préparation du liquide maître DMSO : mg médicament prédissous dans μL DMSO ( Concentration du liquide maître mg/mL, Veuillez nous contacter dabord si la concentration dépasse la solubilité du DMSO du lot de médicament. )
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, ajouter ensuiteμL PEG300, mélanger et clarifier, ajouter ensuiteμL Tween 80, mélanger et clarifier, ajouter ensuite μL ddH2O, mélanger et clarifier.
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, ajouter ensuite μL Huile de maïs, mélanger et clarifier.
Remarque : 1. Assurez-vous que le liquide est clair avant dajouter le solvant suivant.
2. Assurez-vous dajouter le(s) solvant(s) dans lordre. Vous devez vous assurer que la solution obtenue lors de lajout précédent est une solution claire avant de procéder à lajout du solvant suivant. Des méthodes physiques telles que le vortex, les ultrasons ou le bain-marie peuvent être utilisées pour faciliter la dissolution.
Mécanisme daction
| Targets/IC50/Ki |
VEGFR2/KDR
(Cell-free assay) 0.035 nM
c-Met
(Cell-free assay) 1.3 nM
RET
(Cell-free assay) 4 nM
Kit
(Cell-free assay) 4.6 nM
Flt-4
(Cell-free assay) 6 nM
Axl
(Cell-free assay) 7 nM
Flt-3
(Cell-free assay) 11.3 nM
Flt-1
(Cell-free assay) 12 nM
Tie2
(Cell-free assay) 14.3 nM
|
|---|---|
| In vitro |
Le Cabozantinib malate a une faible activité inhibitrice contre RON et PDGFRβ avec un IC50 de 124 nM et 234 nM, respectivement, et a une faible activité contre FGFR1 avec un IC50 de 5,294 μM. Ce composé à faible concentration (0,1-0,5 μM) est suffisant pour induire une inhibition marquée de la phosphorylation constitutive et inductible de Met et de sa signalisation en aval résultante dans les cellules MPNST, et inhiber la migration et l'invasion des cellules MPNST induites par le HGF. Il induit également une inhibition marquée de la phosphorylation de Met et de VEGFR2 dans les cellules endothéliales de la veine ombilicale humaine (HUVECs) stimulées par les cytokines. Bien que cette substance chimique n'ait pas d'effet significatif sur la croissance des cellules MPNST à 0,1 μM, elle inhibe significativement la croissance des cellules MPNST à 5-10 μM.
|
| In vivo |
Le traitement au Cabozantinib malate à 30 mg/kg chez des souris RIP-Tag2 atteintes de tumeurs spontanées des îlots pancréatiques perturbe 83% de la vascularisation tumorale, réduit les péricytes et les manchons de membrane basale vides, provoque une hypoxie intratumorale généralisée et une apoptose étendue des cellules tumorales, et ralentit la repousse de la vascularisation tumorale après le retrait du médicament, plus significativement par rapport à XL999 qui bloque VEGFR mais pas c-Met, entraînant seulement une réduction de 43% de la vascularisation, suggérant qu'une inhibition concurrente de VEGFR et d'autres récepteurs tyrosine kinases (RTK) fonctionnellement pertinents amplifie l'inhibition de l'angiogenèse. Ce composé diminue également l'invasivité des tumeurs primaires et réduit les métastases. Cette substance chimique à 30 mg/kg/jour abroge significativement la croissance et la métastase de xénogreffes de MPNST humaines chez des souris SCID. L'administration de ce composé induit une inhibition dose-dépendante de la croissance tumorale dans des modèles de tumeurs du sein, du poumon et du gliome, en association avec une diminution de la prolifération des cellules tumorales et endothéliales ainsi qu'une augmentation de l'apoptose. Une dose orale unique de cette substance chimique est suffisante pour induire une inhibition soutenue de la croissance tumorale chez des souris porteuses de tumeurs MDA-MB-231 et des rats porteurs de tumeurs C6 à 100 mg/kg et 10 mg/kg, respectivement.
|
Références |
|
Applications
| Méthodes | Biomarqueurs | Images | PMID |
|---|---|---|---|
| Western blot | pROS1 / pERK / pSHP2 / p-STAT3 / p-AKT p-MET / MET / p-ERK5 / ERK5 / DCLK1 |
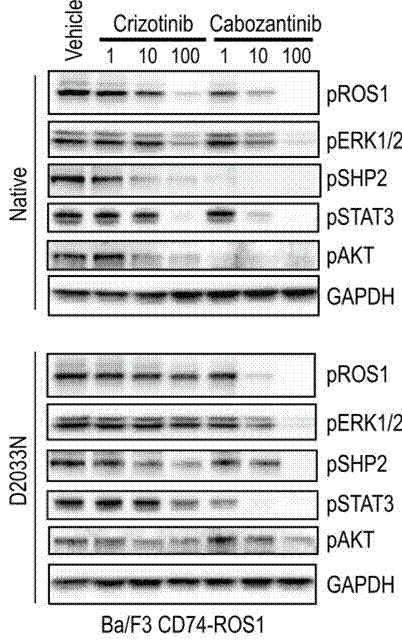
|
26673800 |
| Growth inhibition assay | Cell viability |
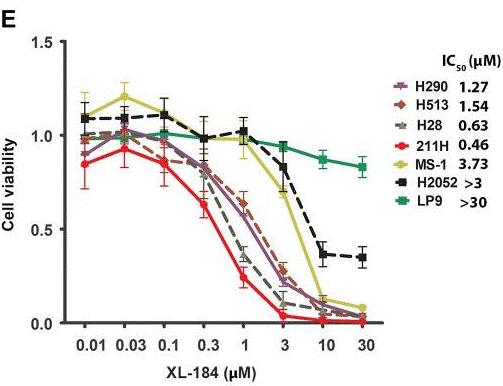
|
28560410 |
Informations sur lessai clinique
(données de https://clinicaltrials.gov, mis à jour le 2024-05-22)
| Numéro NCT | Recrutement | Conditions | Sponsor/Collaborateurs | Date de début | Phases |
|---|---|---|---|---|---|
| NCT06156410 | Recruiting | Ewing Sarcoma|Osteosarcoma |
Children''s Hospital of Philadelphia|Children''s Hospital Colorado|Exelixis|Alex''s Lemonade Stand Foundation |
October 24 2023 | Phase 1 |
| NCT05249114 | Active not recruiting | Neuroendocrine Tumors |
Providence Health & Services|Exelixis|Advanced Accelerator Applications SA |
December 28 2022 | Phase 1 |
| NCT05444933 | Completed | Advanced Renal Cell Carcinoma |
Ipsen |
September 16 2022 | -- |
Support technique
Tel: +1-832-582-8158 Ext:3
Si vous avez dautres questions, veuillez laisser un message.
