Technische gegevens
| Formule | C22H24BrFN4O2 |
||||||
| Moleculair gewicht | 475.35 | CAS-nr. | 443913-73-3 | ||||
| Oplosbaarheid (25°C)* | In vitro | DMSO | 38 mg/mL (79.94 mM) | ||||
| Water | Insoluble | ||||||
| Ethanol | Insoluble | ||||||
| In vivo (Voeg oplosmiddelen afzonderlijk en in volgorde toe aan het product.) |
|
||||||
|
* <1 mg/ml betekent licht oplosbaar of onoplosbaar. * Houd er rekening mee dat Selleck de oplosbaarheid van alle verbindingen intern test en de werkelijke oplosbaarheid enigszins kan afwijken van gepubliceerde waarden. Dit is normaal en is te wijten aan lichte batch-tot-batch variaties. * Verzending op kamertemperatuur (Stabiliteitstests tonen aan dat dit product zonder koelmaatregelen kan worden verzonden.) |
|||||||
Voorbereiden van stamoplossingen
Biologische activiteit
| Beschrijving | Vandetanib is een potente remmer van VEGFR2 met een IC50 van 40 nM in een celvrije assay. Het remt ook VEGFR3 en EGFR met een IC50 van respectievelijk 110 nM en 500 nM. Het is niet gevoelig voor PDGFRβ, Flt1, Tie-2 en FGFR1 met een IC50 van 1,1-3,6 μM. Geen activiteit tegen MEK, CDK2, c-Kit, erbB2, FAK, PDK1, Akt en IGF-1R met een IC50 boven 10 μM. Deze verbinding verhoogt apoptose en induceert autofagie door het niveau van reactieve zuurstofsoorten (ROS) te verhogen. | ||||||
|---|---|---|---|---|---|---|---|
| Doelen |
|
||||||
| In vitro | Vandetanib remt ook VEGFR3 en EGFR met een IC50 van respectievelijk 110 nM en 500 nM. Deze verbinding is niet gevoelig voor PDGFRβ, Flt1, Tie-2 en FGFR1 met een IC50 van 1,1-3,6 μM, terwijl het bijna geen activiteit heeft tegen MEK, CDK2, c-Kit, erbB2, FAK, PDK1, Akt en IGF-1R met een IC50 boven 10 μM. Het remt VEGF-, EGF- en bFGF-gestimuleerde HUVEC-proliferatie met een IC50 van 60 nM, 170 nM en 800 nM, zonder effect op de basale endotheelcelgroei. Deze chemische stof remt de tumorcelgroei met een IC50 van 2,7 μM (A549) tot 13,5 μM (Calu-6). Het vertoont een remmend effect op de basale ABCG2-ATPase. Parentale en ABCG2-expresserende A431-cellen vertoonden vergelijkbare gevoeligheden voor deze verbinding. Blootstelling aan EGFR-remmers vermindert de pEGFR-niveaus in A431-cellen, waarbij deze verbinding slechts een matig effect vertoont. Het vertoont een licht maar meetbaar effect, terwijl gefitinib, pelitinib en neratinib de ABCG2-gemedieerde efflux van mitoxantrone uit A431/ABCG2-cellen volledig remmen, vergelijkbaar met de specifieke ABCG2-remmer Ko143. Het remt zowel PC3wt- als PC3R-cellijnen met vergelijkbare IC50's van respectievelijk 13,3 μM en 11,5 μM. Deze chemische stof onderdrukt de fosforylering van VEGFR2 in HUVEC en EGFR in hepatomacellen en remt celproliferatie. Het veroorzaakt een accumulatie van cellen in de G0-G1-fasen in GEO- en OVCAR-3-cellen en verhoogt apoptose in OVCAR-3, ZR-75-1, MCF-10A ras en GEO-cellen. Deze verbinding veroorzaakt een dosisafhankelijke remming van EGFR-fosforylering in muis NIH-EGFR-fibroblasten en menselijke MCF-10A ras-borstkankercellen, twee cellijnen die de menselijke EGFR overexpressie vertonen. De behandeling resulteert in een dosisafhankelijke remming van zachte agar-groei in zeven menselijke cellijnen (borst, darm, maag en eierstok) met functionele EGFR maar zonder VEGFR2. | ||||||
| In vivo | Vandetanib (2,5 mg/kg, i.v.) keert een VEGF-geïnduceerde hypotensie met 63% om, maar beïnvloedt een bFGF-geïnduceerde hypotensie niet significant. Deze verbinding (100 mg/kg) remt de tumor-geïnduceerde bloedvatvorming met 79%. Het (12,5-100 mg/kg, oraal) vertoont een grote tumorremming in menselijke tumortransplantaten waaronder Calu-6, PC-3, MDA-MA-231, SKOV-3, SW620, A549, A431, B16-F10(AP3) en Lewis Lung, met weinig effecten op het lichaamsgewicht. In PC3wt-xenografts oefent de toediening van deze verbinding alleen paradoxale tumorgroeistimulerende effecten uit. In PC3R-xenografts heeft de lage dosis van deze chemische stof (25 mg/kg) geen significant effect ten opzichte van de controle, terwijl de hoge dosis (50 mg/kg) de tumorgroei significant remt in vergelijking met de controle. Daarentegen onthult de hogedosiscombinatie een significante negatieve interactie tussen deze verbinding 50 mg/kg en docetaxel 30 mg/kg in PC3R-cellen. Bij tumor-dragende muizen onderdrukt het de fosforylering van VEGFR2 en EGFR in tumorweefsels, vermindert het de tumorvatdichtheid significant, verbetert het de tumorcelapoptose, onderdrukt het de tumorgroei, verbetert het de overleving, vermindert het het aantal intrahepatische metastasen en reguleert het VEGF, TGF-alpha en EGF opwaarts in tumorweefsels. Behandeling met deze verbinding is niet geassocieerd met ernstige bijwerkingen, waaronder ALT-afwijkingen, beenmergonderdrukking of gewichtsverlies. Deze chemische behandeling van naakte muizen met palpabele GEO-colonkanker-xenografts (die gevoelig zijn voor remming van EGFR-signalering) induceert dosisafhankelijke tumorgroei-remming. |
Protocol (uit referentie)
| Kinase-assay: |
|
|---|---|
| Celassay: |
|
| Dierstudie: |
|
Referenties
|
Klantproductvalidatie
![<p>Vandetanib reduced extracellular nitrite levels in endothelial cells. MS1 endothelial cells (ECs) were incubated with 1 mol/L of vandetanib or matched vehicle (dimethyl sulfoxide [DMSO]), 50 ng/mL of vascular endothelial growth factor (VEGF) or matched vehicle (PBS; 0.5 hours), and L-arginine and soluble N-ethylmaleamide sensitive factor attachment protein (SNAP) added (1.5 hours). Vandetanib lowered nitrite levels in MS1 Ecs (*P0.0003). VEGF was used a positive control and increased nitrite levels (**P0.02). These findings indicate that vandetanib lowered endothelial cell NO levels.</p>](https://file.selleckchem.com/downloads/review/700px/Vandetanib-Zactima-S104601Z0220100601.gif)
-
Gegevens van [ Hypertension , 2011 , 58, 85-92 ]
![<p>Vandetanib reduced phosphorylation of Akt in endothelial cells (ECs). MS1 ECs were incubated with 1 μmol/L of vandetanib or matched vehicle (dimethyl sulfoxide [DMSO]; 1 hour). Western blotting analysis showed that vandetanib decreased phosphorylation of Akt (S473) in MS1 ECs (*P<0.01; n=6 per group, studies done in triplicate). These findings show that vandetanib reduced Akt activity.</p>](https://file.selleckchem.com/downloads/review/700px/Vandetanib-Zactima-S104601W0320100601.gif)
-
Gegevens van [ Hypertension , 2011 , 58, 85-92 ]
![<p>Vandetanib increases membrane localization of endothelial NO synthase (eNOS). MS1 endothelial cells (ECs) were incubated with 1 μmol/L of vandetanib or matched vehicle (dimethyl sulfoxide [DMSO]). Western blotting analysis showed that vandetanib increases membrane localization of eNOS compared with control (*P<0.04; n=4 per group, studies done in triplicate). These findings show that vandetanib increased the membrane localization of eNOS compared with control.</p>](https://file.selleckchem.com/downloads/review/700px/Vandetanib-Zactima-S104601Z0420100601.gif)
-
Gegevens van [ Hypertension , 2011 , 58, 85-92 ]
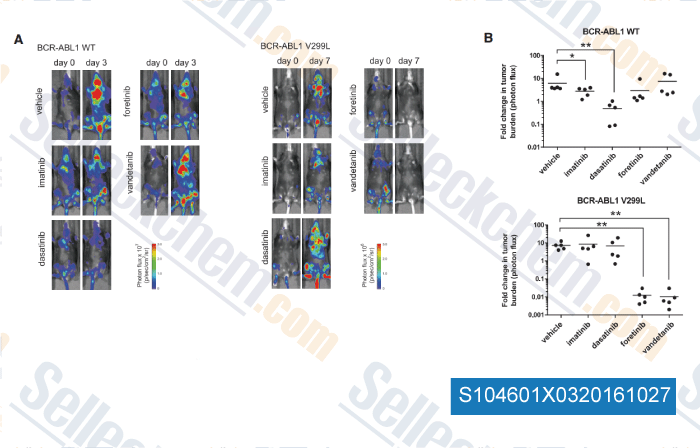
-
, , Cell, 2016, 165(1):234-46.
Sellecks Vandetanib Is geciteerd door 118 Publicaties
| Ponatinib and other clinically approved inhibitors of Src and Rho-A kinases abrogate dengue virus serotype 2- induced endothelial permeability [ Virulence, 2025, 16(1):2489751] | PubMed: 40189910 |
| Kinase Plasticity in Response to Vandetanib Enhances Sensitivity to Tamoxifen in Estrogen Receptor Positive Breast Cancer [ bioRxiv, 2025, 2024.12.19.629395] | PubMed: 39975402 |
| CAVIN1-Mediated hERG Dynamics: A Novel Mechanism Underlying the Interindividual Variability in Drug-Induced Long QT [ Circulation, 2024, 150(7):563-576] | PubMed: 38682330 |
| Novel therapeutic strategies targeting bypass pathways and mitochondrial dysfunction to combat resistance to RET inhibitors in NSCLC [ Biochim Biophys Acta Mol Basis Dis, 2024, 1870(6):167249] | PubMed: 38768929 |
| Patient-derived rhabdomyosarcoma cells recapitulate the genetic and transcriptomic landscapes of primary tumors [ iScience, 2024, 27(10):110862] | PubMed: 39319271 |
| Vandetanib as a prospective anti-inflammatory and anti-contractile agent in asthma [ Front Pharmacol, 2024, 15:1345070] | PubMed: 38799165 |
| ETV2 primes hematoendothelial gene enhancers prior to hematoendothelial fate commitment [ Cell Rep, 2023, 42(6):112665] | PubMed: 37330911 |
| Nuclear translocation of cGAS orchestrates VEGF-A-mediated angiogenesis [ Cell Reports, 2023, 112328] | PubMed: None |
| Nuclear translocation of cGAS orchestrates VEGF-A-mediated angiogenesis [ Cell Rep, 2023, 42(4):112328] | PubMed: 37027305 |
| Phosphate-induced activation of VEGFR2 leads to caspase-9-mediated apoptosis of hypertrophic chondrocytes [ iScience, 2023, 26(9):107548] | PubMed: 37636062 |
RETOURBELEID
Selleck Chemicals onvoorwaardelijke retourbeleid zorgt voor een soepele online winkelervaring voor onze klanten. Als u op enigerlei wijze ontevreden bent met uw aankoop, kunt u elk artikel(en) binnen 7 dagen na ontvangst retourneren. In geval van problemen met de productkwaliteit, zowel protocolgerelateerde als productgerelateerde problemen, kunt u elk artikel(en) binnen 365 dagen na de oorspronkelijke aankoopdatum retourneren. Volg de onderstaande instructies bij het retourneren van producten.
VERZENDING EN OPSLAG
Selleck producten worden bij kamertemperatuur vervoerd. Als u het product op kamertemperatuur ontvangt, wees dan gerust, de Selleck kwaliteitsinspectieafdeling heeft experimenten uitgevoerd om te controleren of de normale temperatuurplaatsing van één maand de biologische activiteit van poederproducten niet beïnvloedt. Na ontvangst dient u het product op te slaan volgens de vereisten beschreven in het gegevensblad. De meeste Selleck producten zijn stabiel onder de aanbevolen omstandigheden.
NIET VOOR HUMANE, VETERINAIRE DIAGNOSTISCHE OF THERAPEUTISCHE DOELEINDEN.
