Technische gegevens
| Formule | C21H22Cl2FN5O |
||||||||||||||
| Moleculair gewicht | 450.34 | CAS-nr. | 877399-52-5 | ||||||||||||
| Oplosbaarheid (25°C)* | In vitro | DMSO | 25 mg/mL (55.51 mM) | ||||||||||||
| Water | Insoluble | ||||||||||||||
| Ethanol | Insoluble | ||||||||||||||
| In vivo (Voeg oplosmiddelen afzonderlijk en in volgorde toe aan het product.) |
|
||||||||||||||
|
* <1 mg/ml betekent licht oplosbaar of onoplosbaar. * Houd er rekening mee dat Selleck de oplosbaarheid van alle verbindingen intern test en de werkelijke oplosbaarheid enigszins kan afwijken van gepubliceerde waarden. Dit is normaal en is te wijten aan lichte batch-tot-batch variaties. * Verzending op kamertemperatuur (Stabiliteitstests tonen aan dat dit product zonder koelmaatregelen kan worden verzonden.) |
|||||||||||||||
Voorbereiden van stamoplossingen
Biologische activiteit
| Beschrijving | Crizotinib is een krachtige remmer van c-Met en ALK met IC50 van respectievelijk 11 nM en 24 nM in celgebaseerde assays. Het is ook een krachtige ROS1 remmer met een Ki-waarde van minder dan 0,025 nM. Crizotinib induceert autofagie door remming van de STAT3-route in meerdere longkankercellijnen. | ||||||
|---|---|---|---|---|---|---|---|
| Doelen |
|
||||||
| In vitro | PF-2341066 vertoont vergelijkbare potentie tegen c-Met-fosforylering in mIMCD3 muizen- of MDCK hondenepitheelcellen met IC50 van respectievelijk 5 nM en 20 nM. Deze verbinding vertoont verbeterde of vergelijkbare activiteit tegen NIH3T3-cellen die zijn gemanipuleerd om c-Met ATP-bindingsplaatsmutanten V1092I of H1094R of de P-loop-mutant M1250T tot expressie te brengen met IC50 van respectievelijk 19 nM, 2 nM en 15 nM, vergeleken met NIH3T3-cellen die de wildtype-receptor tot expressie brengen met IC50 van 13 nM. Daarentegen wordt een duidelijke verschuiving in potentie van deze verbinding waargenomen tegen cellen die zijn gemanipuleerd om c-Met-activeringslusmutanten Y1230C en Y1235D tot expressie te brengen met IC50 van respectievelijk 127 nM en 92 nM, vergeleken met de wildtype-receptor. Het voorkomt ook krachtig de fosforylering van c-Met in NCI-H69- en HOP92-cellen, met IC50 van respectievelijk 13 nM en 16 nM, die de endogene c-Met-varianten R988C en T1010I tot expressie brengen. Deze verbinding is >1.000-voudig selectief voor de VEGFR2- en PDGFRβ RTK's, >250-voudig selectief voor IRK en Lck, en ∼40- tot 60-voudig selectief voor Tie2, TrkA en TrkB, dit alles vergeleken met c-Met. Het is 20- tot 30-voudig selectief voor RON- en Axl RTK's. Daarentegen vertoont deze verbinding een bijna equivalente IC50 van 24 nM tegen de nucleofosmine (NPM)-anaplastische lymfoomkinase (ALK) oncogene fusievariant van de ALK RTK die tot expressie wordt gebracht door de KARPAS299 menselijke anaplastische grootcellige lymfoom (ALCL) cellijn. Het remt c-Met-afhankelijke neoplastische fenotypes van kankercellen en angiogene fenotypes van endotheelcellen. Deze chemische stof onderdrukt de groei van menselijke GTL-16 maagcarcinoomcellen met een IC50 van 9,7 nM. Het induceert apoptose in GTL-16-cellen met een IC50 van 8,4 nM. Het remt HGF-gestimuleerde migratie en invasie van menselijke NCI-H441 longcarcinoomcellen met IC50 van respectievelijk 11 nM en 6,1 nM. Het remt MDCK-celverstrooiing met een IC50 van 16 nM. Het voorkomt HGF-gestimuleerde c-Met-fosforylering, celoverleving en Matrigel-invasie met IC50 van respectievelijk 11 nM, 14 nM en 35 nM. Bovendien voorkomt het serum-gestimuleerde HMVEC-vertakkende tubulogenese (vorming van vasculaire buizen) in fibrinegels. Het remt ook krachtig NPM-ALK-fosforylering in Karpas299- of SU-DHL-1 ALCL-cellen met een IC50 van 24 nM. Deze verbinding voorkomt krachtig celproliferatie, wat gepaard gaat met G(1)-S-fase celcyclusarrest en inductie van apoptose in ALK-positieve ALCL-cellen met IC50 van 30 nM, maar niet in ALK-negatieve lymfoomcellen. Bovendien voorkomt het osteosarcoomgedrag geassocieerd met primaire tumorgroei (d.w.z. proliferatie en overleving) en metastase (bijv. invasie en clonogeniteit). |
||||||
| In vivo | In het GTL-16-model toont PF-2341066 het vermogen om een duidelijke regressie van grote gevestigde tumoren (>600 mm3) te veroorzaken in zowel de 50 mg/kg/dag als de 75 mg/kg/dag behandelingscohorten, met een afname van 60% in het gemiddelde tumorvolume gedurende het 43-daagse toedieningsschema. In een andere studie toont deze verbinding het vermogen om de GTL-16-tumorgroei gedurende >3 maanden volledig te remmen, waarbij slechts 1 van de 12 muizen een significante toename van de tumorgroei vertoonde gedurende het 3-maandse behandelingsschema van 50 mg/kg/dag. In het NCI-H441 NSCLC-model wordt een afname van 43% in het gemiddelde tumorvolume waargenomen bij 50 mg/kg/dag gedurende de 38-daagse PF-2341066-toedieningscyclus. In het Caki-1 RCC-model wordt een afname van 53% in het gemiddelde tumorvolume waargenomen, geassocieerd met een afname van het volume van elke tumor met ten minste 30% bij 50 mg/kg/dag gedurende de 33-daagse PF-2341066-toedieningscyclus. Deze verbinding toont ook een bijna volledige preventie van de groei van gevestigde tumoren bij 50 mg/kg/dag in de U87MG-glioblastoom- of PC-3-prostaatcarcinoom-xenograftmodellen, met respectievelijk 97% of 84% remming op de laatste studiedag. Daarentegen remt deze chemische stof, oraal toegediend bij 50 mg/kg/dag, de tumorgroei niet significant in het MDA-MB-231-borstcarcinoommodel of het DLD-1-coloncarcinoommodel. Een significante dosisafhankelijke reductie van CD31-positieve endotheelcellen wordt waargenomen bij 12,5 mg/kg/dag, 25 mg/kg/dag en 50 mg/kg/dag in GTL-16-tumoren, wat aangeeft dat remming van MVD een dosisafhankelijke correlatie vertoont met antitumorale werkzaamheid. Deze verbinding vertoont een significante dosisafhankelijke reductie van menselijke VEGFA- en IL-8-plasmaspiegels in zowel de GTL-16- als U87MG-modellen. Een duidelijke remming van gefosforyleerde c-Met-, Akt-, Erk-, PLCλ1- en STAT5-niveaus wordt waargenomen in GTL-16-tumoren na orale toediening van deze verbinding. Orale toediening van deze chemische stof aan severe gecombineerde immunodeficiënte-beige muizen met Karpas299 ALCL-tumorxenografts leidt tot dosisafhankelijke antitumorale werkzaamheid met volledige regressie van alle tumoren bij de dosis van 100 mg/kg/dag binnen 15 dagen na de initiële toediening van de verbinding. Bovendien wordt de remming van belangrijke NPM-ALK-signaleringsmediatoren, waaronder fosfolipase C-gamma, signaaltransducers en activatoren van transcriptie 3, extracellulaire signaal-gereguleerde kinasen en Akt door deze verbinding waargenomen bij concentraties of dosisniveaus die correleerden met remming van NPM-ALK-fosforylering en -functie. Deze verbinding voorkomt osteosarcoomgedrag geassocieerd met primaire tumorgroei (bijv. proliferatie en overleving) en metastase (bijv. invasie en clonogeniteit). Bij naakte muizen behandeld met deze chemische stof via orale sondevoeding, worden de groei en geassocieerde osteolyse en extracorticale botmatrixvorming van osteosarcoomxenografts voorkomen door deze verbinding. Behandeling van c-MET-geamplificeerde GTL-16-xenografts met 50 mg/kg van deze verbinding veroorzaakt tumorregressie die geassocieerd is met een langzame vermindering van 18F-FDG-opname en een afname van de expressie van de glucosetransporter 1, GLUT-1. |
Protocol (uit referentie)
| Kinase-assay: |
|
|---|---|
| Celassay: |
|
| Dierstudie: |
|
Referenties
|
Klantproductvalidatie
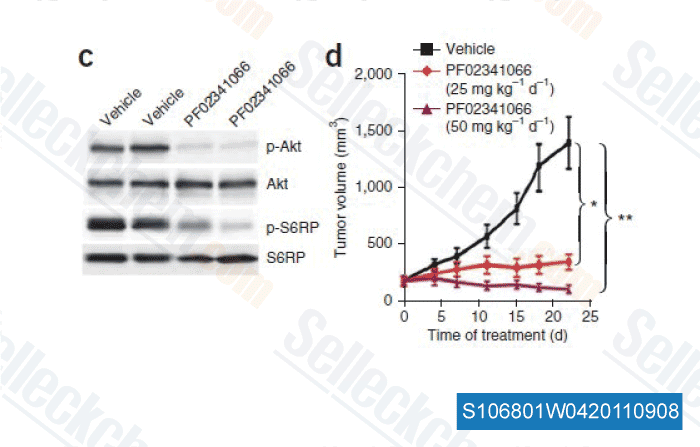
-
Gegevens van [ Nat Med , 2011 , 17, 1116-1120 ]
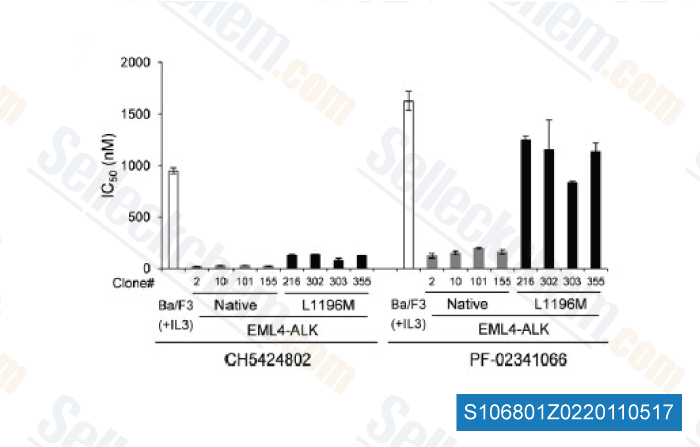
-
Gegevens van [ Cancer Cell , 2011 , 19, 679–690 ]
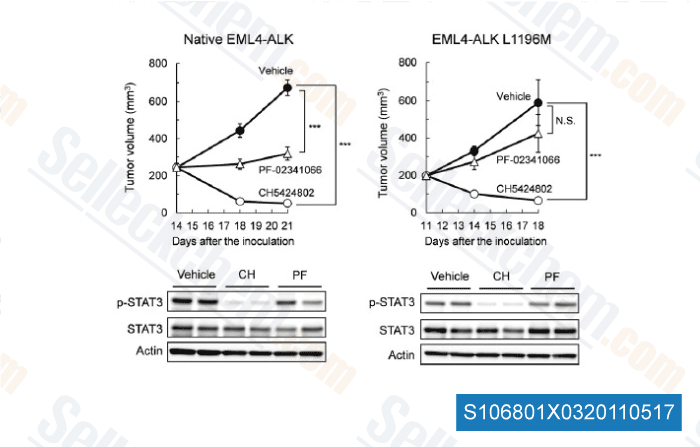
-
Gegevens van [ Cancer Cell , 2011 , 19, 679–690 ]

-
Gegevens van [ J Biomol Screen , 2011 , 16, 141-154 ]
Sellecks PF-02341066 (Crizotinib) Is geciteerd door 499 Publicaties
| RNase1-driven ALK-activation is an oncogenic driver and therapeutic target in non-small cell lung cancer [ Signal Transduct Target Ther, 2025, 10(1):124] | PubMed: 40246819 |
| A patient-derived T cell lymphoma biorepository uncovers pathogenetic mechanisms and host-related therapeutic vulnerabilities [ Cell Rep Med, 2025, S2666-3791(25)00102-8] | PubMed: 40147445 |
| ARID1A loss enhances sensitivity to c-MET inhibition by dual targeting of GPX4 and iron homeostasis, inducing ferroptosis [ Cell Death Differ, 2025, 10.1038/s41418-025-01510-x] | PubMed: 40369167 |
| Targeting proteostasis in multiple myeloma through inhibition of LTK [ Leukemia, 2025, 10.1038/s41375-025-02682-8] | PubMed: 40634511 |
| Multi-layer stratified oncology platform utilizing transcriptomics, prostate cancer organoids, and modeling of drug response [ J Exp Clin Cancer Res, 2025, 44(1):290] | PubMed: 41094672 |
| Novel selective strategies targeting the BCL-2 family to enhance clinical efficacy in ALK-rearranged non-small cell lung cancer [ Cell Death Dis, 2025, 16(1):194] | PubMed: 40113795 |
| The Src family kinase inhibitor drug Dasatinib and glucocorticoids display synergistic activity against tongue squamous cell carcinoma and reduce MET kinase activity [ Cell Commun Signal, 2025, 23(1):293] | PubMed: 40537792 |
| MET variants with activating N-lobe mutations identified in hereditary papillary renal cell carcinomas still require ligand stimulation [ Mol Oncol, 2025, 19(8):2366-2387] | PubMed: 39980226 |
| Synergistic effects of oncogene inhibition and pyruvate dehydrogenase kinase blockade in resistant NSCLC cells [ Biochim Biophys Acta Mol Basis Dis, 2025, 1871(8):168014] | PubMed: 40784600 |
| HGF Overexpression in Mesenchymal Stromal Cell-Based Cell Sheets Enhances Autophagy-Dependent Cytoprotection and Proliferation to Guard the Epicardial Mesothelium [ Int J Mol Sci, 2025, 26(15)7298] | PubMed: 40806435 |
RETOURBELEID
Selleck Chemicals onvoorwaardelijke retourbeleid zorgt voor een soepele online winkelervaring voor onze klanten. Als u op enigerlei wijze ontevreden bent met uw aankoop, kunt u elk artikel(en) binnen 7 dagen na ontvangst retourneren. In geval van problemen met de productkwaliteit, zowel protocolgerelateerde als productgerelateerde problemen, kunt u elk artikel(en) binnen 365 dagen na de oorspronkelijke aankoopdatum retourneren. Volg de onderstaande instructies bij het retourneren van producten.
VERZENDING EN OPSLAG
Selleck producten worden bij kamertemperatuur vervoerd. Als u het product op kamertemperatuur ontvangt, wees dan gerust, de Selleck kwaliteitsinspectieafdeling heeft experimenten uitgevoerd om te controleren of de normale temperatuurplaatsing van één maand de biologische activiteit van poederproducten niet beïnvloedt. Na ontvangst dient u het product op te slaan volgens de vereisten beschreven in het gegevensblad. De meeste Selleck producten zijn stabiel onder de aanbevolen omstandigheden.
NIET VOOR HUMANE, VETERINAIRE DIAGNOSTISCHE OF THERAPEUTISCHE DOELEINDEN.
