uitsluitend voor onderzoeksdoeleinden
Capsazepine TRP Channel antagonist
Cat.Nr.S8137
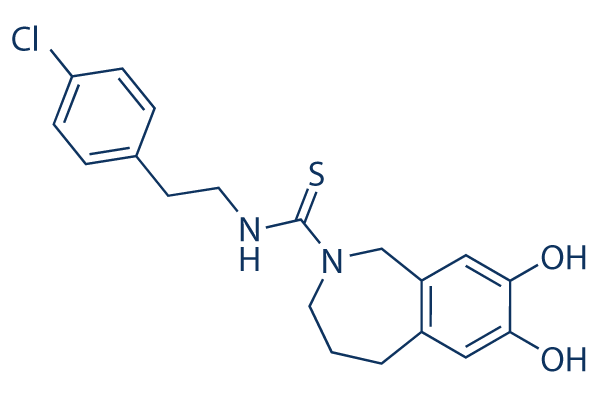
Chemische structuur
Moleculair gewicht: 376.90
Kwaliteitscontrole
| Gerelateerde doelwitten | CFTR CRM1 CD markers AChR Calcium Channel Sodium Channel Potassium Channel GABA Receptor ATPase GluR |
|---|---|
| Overige TRP Channel Inhibitoren | 2-APB (2-Aminoethyl Diphenylborinate) SKF96365 AMG-517 GSK2193874 GSK1016790A HC-030031 EIPA (L593754) SB705498 HC-067047 ML-SI3 |
Celkweek, behandeling & werkconcentratie
| Cellijnen | Assaytype | Concentratie | Incubatietijd | Formulering | Activiteitsbeschrijving | PMID |
|---|---|---|---|---|---|---|
| CHO | Function assay | Inhibition of capsaicin-induced [Ca2+] uptake by Rat Vanilloid receptor 1 (VR1) expressing CHO cells, Ki=0.52μM | 12825950 | |||
| CHO | Function assay | Inhibition of capsaicin-induced calcium uptake by transient receptor potential vanilloid type 1 expressed in CHO cells, IC50=0.42μM | 15634002 | |||
| CHO | Function assay | Antagonist activity towards rat TRPV1 expressed in CHO cells, Ki=0.52μM | 15993063 | |||
| CHO | Function assay | In vitro inhibition of [3H]RTX binding to rat TRPV1 expressed in CHO cells, Ki=1.3μM | 15993063 | |||
| HEK293 | Function assay | Inhibition of 100 nM capsaicin effect on intracellular [Ca2+] concentration in HEK293 cells expressing human TRPV1, IC50=0.0562μM | 16000002 | |||
| CHO | Function assay | Antagonist activity for rat TRPV1 expressed in CHO cells, Ki=0.52μM | 16005215 | |||
| CHO | Function assay | In vitro binding affinity for rat TRPV1 expressed in CHO cells using [3H]-RTX, Ki=1.3μM | 16005215 | |||
| human TRPV1 expressing cells | Function assay | Inhibition of calcium influx evoked by capsaicin in human TRPV1 expressing cells by fluorescence assay, IC50=0.334μM | 16420034 | |||
| CHO | Function assay | Antagonist activity at rat TRPV1 expressed in CHO cells assessed as inhibition of calcium uptake, Ki=0.52μM | 17035013 | |||
| CHO | Function assay | Displacement of [3H]RTX from rat TRPV1 expressed in CHO cells, Ki=1.3μM | 17035013 | |||
| CHO | Function assay | Antagonist activity at human TRPV1 expressed in CHO cells assessed as blockade of capsaicin-induced receptor activation by aequorin based assay, IC50=0.039μM | 17489570 | |||
| CHO | Function assay | Antagonist activity at human TRPV1 expressed in CHO cells assessed as blockade of capsaicin-induced receptor activation by [45Ca2+] uptake assay, IC50=0.053μM | 17489570 | |||
| CHO | Function assay | Antagonist activity at human TRPV1 expressed in CHO cells assessed as blockade of acid-induced receptor activation by [45Ca2+] uptake assay, IC50=0.069μM | 17489570 | |||
| CHO | Function assay | Antagonist activity at rat TRPV1 expressed in CHO cells assessed as blockade of capsaicin-induced receptor activation by aequorin based assay, IC50=0.22μM | 17489570 | |||
| CHO | Function assay | Antagonist activity at human TRPV1 expressed in CHO cells assessed as blockade of acid-induced receptor activation by aequorin based assay, IC50=0.32μM | 17489570 | |||
| CHO | Function assay | Antagonist activity at rat TRPV1 expressed in CHO cells assessed as blockade of capsaicin-induced receptor activation by [45Ca2+] uptake assay, IC50=0.887μM | 17489570 | |||
| CHO | Function assay | Antagonist activity at rat TRPV1 receptor expressed in CHO cells assessed as calcium 45 uptake, Ki=0.52μM | 18072720 | |||
| CHO | Function assay | Displacement of [3H]RTX from rat TRPV1 receptor expressed in CHO cells, Ki=1.3μM | 18072720 | |||
| HEK293 | Function assay | Antagonist activity at human TRPV1 expressed in tetracycline-stimulated HEK293 cells assessed as inhibition of capsaicin-induced intracellular calcium levels by fluorimetric assay, EC50=2.51189μM | 20381363 | |||
| HEK293T | Function assay | Antagonist activity at human brain TRPV1 expressed in HEK293T cells assessed as inhibition of CAP-induced intracellular Ca2+ influx by fluorescence-based assay, IC50=0.15μM | 24484240 | |||
| HEK293T | Function assay | 10 uM | Antagonist activity at human brain TRPV1 expressed in HEK293T cells assessed as inhibition of proton-induced intracellular Ca2+ influx at 10 uM by fluorescence-based assay | 24484240 | ||
| HEK T-REx cells | Function assay | >50 uM | Antagonist at TRPM8 isolated from mouse dorsal root ganglion cells expressed in HEK T-REx cells assessed as inhibition of icilin-induced intracellular Ca2+ influx at >50 uM by fluorescence-based assay | 24484240 | ||
| HEK293T | Function assay | 100 uM | Antagonist activity at human brain TRPV1 expressed in HEK293T cells assessed as inhibition of proton-induced intracellular Ca2+ influx at 100 uM by fluorescence-based assay | 24484240 | ||
| T-REx HEK cells | Function assay | 3 mins | Antagonist activity against human TRPV1 expressed in T-REx HEK cells assessed as inhibition of capsaicin-induced increase in intracellular Ca2+ accumulation pre-incubated for 3 mins prior to capsaicin stimulation by Fluo-4 AM dye based fluorescence assay, IC50=0.068μM | 25052206 | ||
| T-REx HEK cells | Function assay | 3 mins | Antagonist activity against mouse TRPM8 expressed in T-REx HEK cells assessed as inhibition of cold-induced increase in intracellular Ca2+ accumulation pre-incubated for 3 mins prior to cold stimulation by Fluo-4 AM dye based fluorescence assay | 25052206 | ||
| HeLa | Antiproliferative assay | 24 hrs | Antiproliferative activity against human HeLa cells after 24 hrs by cell titer 96 aqueous non-radioactive cell proliferation assay, IC50=30μM | 30528162 | ||
| Klik om meer experimentele gegevens over de cellijn te bekijken | ||||||
Chemische informatie, Opslag en Stabiliteit
| Moleculair gewicht | 376.90 | Formule | C19H21ClN2O2S |
Opslag (Vanaf de ontvangstdatum) | |
|---|---|---|---|---|---|
| CAS-nr. | 138977-28-3 | SDF downloaden | Opslag van stamoplossingen |
|
|
| Synoniemen | N/A | Smiles | C1CC2=CC(=C(C=C2CN(C1)C(=S)NCCC3=CC=C(C=C3)Cl)O)O | ||
Oplosbaarheid
|
In vitro |
DMSO
: Insoluble
Water : Insoluble Ethanol : Insoluble |
Molariteitscalculator
|
In vivo |
|||||
In vivo Formuleringscalculator (Heldere oplossing)
Stap 1: Voer de onderstaande informatie in (Aanbevolen: Een extra dier voor het geval van verlies tijdens het experiment)
Stap 2: Voer de in vivo formulering in (Dit is alleen de calculator, geen formulering. Neem eerst contact met ons op als er geen in vivo formulering is in het gedeelte Oplosbaarheid.)
Berekeningsresultaten:
Werkconcentratie: mg/ml;
Methode voor het bereiden van DMSO-mastervloeistof: mg geneesmiddel vooraf opgelost in μL DMSO ( Concentratie mastervloeistof mg/mL, Neem eerst contact met ons op als de concentratie de DMSO-oplosbaarheid van de partij geneesmiddel overschrijdt. )
Methode voor het bereiden van in vivo formulering: Neem μL DMSO mastervloeistof, voeg vervolgens toeμL PEG300, mengen en helder maken, voeg vervolgens toeμL Tween 80, mengen en helder maken, voeg vervolgens toe μL ddH2O, mengen en helder maken.
Methode voor het bereiden van in vivo formulering: Neem μL DMSO mastervloeistof, voeg vervolgens toe μL Maïsolie, mengen en helder maken.
Opmerking: 1. Zorg ervoor dat de vloeistof helder is voordat u het volgende oplosmiddel toevoegt.
2. Zorg ervoor dat u het/de oplosmiddel(en) in de juiste volgorde toevoegt. U moet ervoor zorgen dat de verkregen oplossing, bij de vorige toevoeging, een heldere oplossing is voordat u verdergaat met het toevoegen van het volgende oplosmiddel. Fysische methoden zoals vortexen, echografie of een warmwaterbad kunnen worden gebruikt om het oplossen te bevorderen.
Werkingsmechanisme
| Targets/IC50/Ki |
TRPV1
Na,K-ATPase
12 μM(EC50)
|
|---|---|
| In vitro |
Capsazepine(CPZ) in een concentratie van 94,2 µg/ml (IC50-concentratie van deze verbinding) vertoont een statistisch significante remming van de groei en proliferatie van osteoclasten. Deze verbinding zet de NKA om in Na-ATPase. Het remt de K+-afhankelijke activiteit, maar laat Na-ATPase geassocieerd met Na+-transport toe. CPZ heeft geen effect op Na-ATPase gemeten in afwezigheid van K+. Deze chemische stof remt ook de para-nitrofenylfosfatase-activiteit, zij het met een lagere affiniteit. Het vermindert sterk het steady-state EP-niveau en de Na+-affiniteit voor fosforylering nam 3-voudig af na CPZ-behandeling. Kortom, deze verbinding blokkeert een Na+/K+-cyclus in de NKA, maar laat een Na+-cyclus intact, waardoor de transportstoichiometrie van de pomp wordt verminderd. Deze chemische stof remt de osteoclastvorming en botresorptie op een dosisafhankelijke manier in beenmerg-osteoblast co-culturen en RANKL-gegenereerde osteoclastculturen. Het onderdrukt ook RANKL-geïnduceerde IκB- en ERK1/2-fosforylering en veroorzaakt apoptose van rijpe osteoclasten en remt ook alkalische fosfatase-activiteit en botnodulusvorming in calvariale osteoblastculturen. |
| In vivo |
Voorbehandeling met Capsazepine voorkomt de toename van de weerstand van het ademhalingssysteem en vermindert de toename van weefseldemping tijdens endotoxemie. Deze verbinding vermindert ook longletsel door een vermindering van het samengevallen gebied van het longparenchym, geïnduceerd door lipopolysaccharide (LPS). |
Referenties |
|
Technische ondersteuning
Tel: +1-832-582-8158 Ext:3
Als u nog andere vragen heeft, kunt u een bericht achterlaten.
