Données techniques
| Formule | C21H16N6O2S2 |
||||||||||
| Poids moléculaire | 448.52 | N° CAS | 956958-53-5 | ||||||||
| Solubilité (25°C)* | In vitro | DMSO | 90 mg/mL (200.65 mM) | ||||||||
| Water | Insoluble | ||||||||||
| Ethanol | Insoluble | ||||||||||
| In Vivo (Ajoutez les solvants au produit individuellement et dans lordre.) |
|
||||||||||
|
* <1 mg/ml signifie légèrement soluble ou insoluble. * Veuillez noter que Selleck teste la solubilité de tous les composés en interne, et la solubilité réelle peut différer légèrement des valeurs publiées. Ceci est normal et est dû à de légères variations dun lot à lautre. * Expédition à température ambiante (les tests de stabilité montrent que ce produit peut être expédié sans aucune mesure de refroidissement.) |
|||||||||||
Préparation des solutions mères
Activité biologique
| Description | Le XL147 analogue (SAR245408) est un inhibiteur sélectif et réversible de la classe I de PI3K pour PI3Kα/δ/γ avec un IC50 de 39 nM/36 nM/23 nM dans les essais sans cellules, moins puissant pour PI3Kβ. Ce composé induit l'apoptose. Phase 1/2. | ||||||||
|---|---|---|---|---|---|---|---|---|---|
| Cibles |
|
||||||||
| In vitro | Le XL147 analogue inhibe les isoformes de la classe I de PI3K de manière compétitive à l'ATP. Dans un panel de lignées cellulaires de cancer du sein humain surexprimant HER2, le traitement avec ce composé abroge la phosphorylation d'AKT et de S6, mais induit également l'expression et la phosphorylation de HER3 et d'autres RTK. Dans les cellules HER2+, la phosphorylation de HER3 est maintenue par la tyrosine kinase HER2, ce qui conduit à une récupération partielle d'AKT phosphorylé (pAKT) et limite ainsi l'action antitumorale de cette substance chimique. De plus, le silençage de HER3 ou le traitement avec les agents anti-HER2 trastuzumab ou lapatinib sensibilise les cellules de cancer du sein HER2+ à cet agent in vitro et in vivo. Le traitement avec cet inhibiteur inhibe la croissance en monocouche de toutes les lignées cellulaires testées, y compris BT474, HCC1937 et al., de manière dose-dépendante. L'effet principal de ce composé est l'inhibition de la prolifération cellulaire. Il induit la mort cellulaire à une concentration de 20 μM. Le traitement avec cette substance chimique conduit à une inhibition dose-dépendante de PI3K. Conformément à l'inhibition de la prolifération cellulaire, il induit une réduction de la cycline D1 et de pRB et une augmentation des niveaux de l'inhibiteur de CDK p27KIPI, mais aucun changement détectable dans les niveaux de poly(ADP-ribose) polymérase (PARP) totale ou clivée. Le traitement avec cet agent entraîne une réduction dose-dépendante de pAKTS473/T308 et pS6S240/244. Étonnamment, il déclenche également une surexpression des niveaux totaux de HER3 et/ou de pHER3Y1289. Dans les cellules surexprimant HER2, l'inhibition de PI3K est suivie d'une surexpression de l'expression et de la phosphorylation de plusieurs récepteurs tyrosine kinases, y compris HER3. Le silençage des facteurs de transcription FoxO1 et FoxO3a empêche l'induction des ARNm de HER3, InsR, IGF1R et FGFR2 lors de l'inhibition de PI3K. Dans les cellules HER2+, le silençage de HER3 avec un siRNA ou un cotraitement avec les inhibiteurs de HER2 trastuzumab ou lapatinib améliore la mort cellulaire induite par XL147 et l'inhibition de pAKT et pS6. | ||||||||
| In Vivo | Des souris athymiques avec des xénogreffes BT474 sont traitées aléatoirement avec le XL147 analogue, le lapatinib, le trastuzumab, ou ce composé plus chaque antagoniste de HER2. Chaque monothérapie inhibe significativement la croissance tumorale, le trastuzumab étant le seul agent à induire une régression tumorale complète chez une des huit souris. Les deux combinaisons sont supérieures aux médicaments respectifs administrés seuls. Notamment, la combinaison de trastuzumab et de cette substance chimique, mais pas le lapatinib et le XL147, induit une réponse tumorale complète chez trois des huit souris. Aucune toxicité médicamenteuse marquée n'est observée dans aucun des bras de traitement. La combinaison de ce composé plus le trastuzumab prévient pHER3 plus puissamment que n'importe quel autre traitement. En bon accord avec les différences de croissance tumorale entre les bras de traitement, le pAKT nucléaire est plus faible dans les tumeurs traitées avec XL147 plus lapatinib ou cette substance chimique plus trastuzumab par rapport aux tumeurs traitées avec des agents seuls. Parmi les trois médicaments seuls, ce composé est le seul à avoir montré statistiquement une répression des niveaux de pAKT nucléaire. Aucune modification détectable des niveaux de pAKT cytoplasmique n'est observée. L'inhibition combinée de HER2 et de PI3K dans les xénogreffes dépendantes de HER2 est nécessaire pour inhiber au maximum la sortie de signal de la voie PI3K/AKT. |
Protocole (de référence)
| Test cellulaire : |
|
|---|---|
| Étude animale : |
|
Références
|
Validation du produit par le client
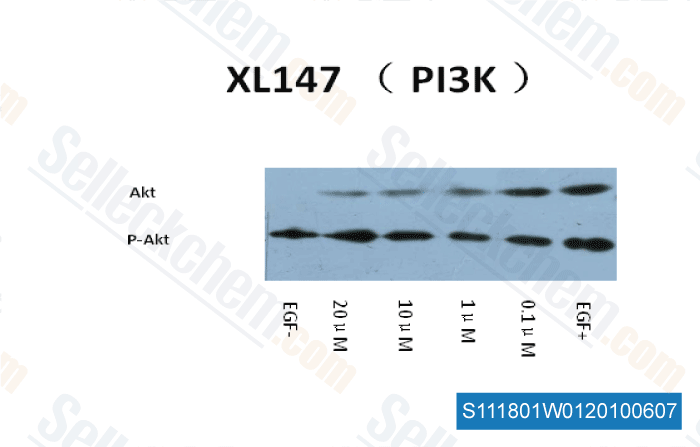
-
Dr. Zhang of Tianjin Medical University ,
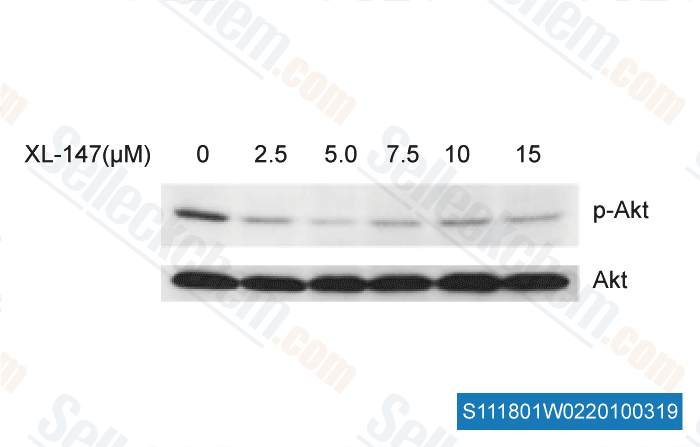
-
, , Dr. Chunrong Yu of RoswelI Park Cancer Institute
De Selleck XL147 analogue A été cité par 11 Publications
| Establishment and Characterization of NCC-PMP1-C1: A Novel Patient-Derived Cell Line of Metastatic Pseudomyxoma Peritonei [ J Pers Med, 2022, 12(2)258] | PubMed: 35207746 |
| Establishment and characterization of NCC-UPS4-C1: a novel cell line of undifferentiated pleomorphic sarcoma from a patient with Li-Fraumeni syndrome [ Hum Cell, 2022, 10.1007/s13577-022-00671-y] | PubMed: 35118583 |
| Establishment and characterization of novel patient-derived cell lines from giant cell tumor of bone [ Hum Cell, 2021, 10.1007/s13577-021-00579-z] | PubMed: 34304386 |
| Establishment and characterization of the NCC-GCTB4-C1 cell line: a novel patient-derived cell line from giant cell tumor of bone [ Hum Cell, 2021, 10.1007/s13577-021-00639-4] | PubMed: 34731453 |
| Establishment and characterization of NCC-MFS4-C1: a novel patient-derived cell line of myxofibrosarcoma [ Hum Cell, 2021, 34(6):1911-1918] | PubMed: 34383271 |
| Establishment and characterization of NCC-MFS2-C1: a novel patient-derived cancer cell line of myxofibrosarcoma [ Hum Cell, 2020, 10.1007/s13577-020-00420-z] | PubMed: 32870449 |
| hMENA11a contributes to HER3-mediated resistance to PI3K inhibitors in HER2-overexpressing breast cancer cells. [Trono P,et al. Oncogene, 2015, 10.1038/onc.2015.143] | PubMed: 25961924 |
| Quantitative optical imaging of primary tumor organoid metabolism predicts drug response in breast cancer [Walsh AJ, et al Cancer Res, 2014, 74(18):5184-94] | PubMed: 25100563 |
| Deciphering Combinations of PI3K/AKT/mTOR Pathway Drugs Augmenting Anti-Angiogenic Efficacy In Vivo [Sasore T, et al PLoS One, 2014, 9(8):e105280] | PubMed: 25144531 |
| Secretory phospholipase A2-IIa upregulates HER/HER2-elicited signaling in lung cancer cells [Axelrod MJ, et al. Head Neck, 2014, 10.1002/hed.23822] | PubMed: 24986420 |
POLITIQUE DE RETOUR
La politique de retour inconditionnelle de Selleck Chemical garantit une expérience dachat en ligne fluide à nos clients. Si vous nêtes en aucun cas satisfait de votre achat, vous pouvez retourner tout article dans les 7 jours suivant sa réception. En cas de problèmes de qualité du produit, quil sagisse de problèmes liés au protocole ou au produit, vous pouvez retourner tout article dans les 365 jours suivant la date dachat initiale. Veuillez suivre les instructions ci-dessous lors du retour des produits.
EXPÉDITION ET STOCKAGE
Les produits Selleck sont transportés à température ambiante. Si vous recevez le produit à température ambiante, soyez assuré que le service dinspection de la qualité de Selleck a mené des expériences pour vérifier que le placement à température normale pendant un mois naffectera pas lactivité biologique des produits en poudre. Après réception, veuillez stocker le produit conformément aux exigences décrites dans la fiche technique. La plupart des produits Selleck sont stables dans les conditions recommandées.
NON DESTINÉ À UN USAGE HUMAIN, VÉTÉRINAIRE DIAGNOSTIQUE OU THÉRAPEUTIQUE.
